Hépato-Gastro & Oncologie Digestive
MENUIron deficiency in digestive oncology Volume 26, supplement 1, Octobre 2019
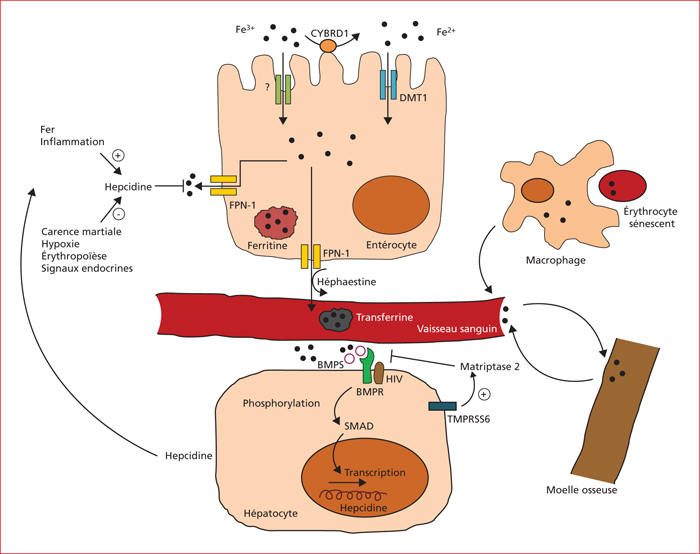
Figure 1
Le fer alimentaire est disponible sous deux formes : héminique (Fe2+) et non héminique (Fe3+). Ce dernier est directement absorbé par l’entérocyte, mais par un transporteur inconnu. Le fer héminique est internalisé et exporté vers le cytosol grâce au DMT1 (divalent metal transporter 1). Le Fe3+ peut être réduit en Fe2+ par la ferrireductase membranaire CYBRD1. Une fois dans l’entérocyte, le fer peut être stocké sous forme de ferritine. L’exportation sanguine du fer se fait par la ferroportine FPN1. Le fer ferrique est finalement lié à la transferrine grâce à l’héphaestine. L’hepcidine régule l’expression de surface de la FPN1, en se liant à elle, entraînant son internalisation et sa dégradation lyzosomale. Le fer circulant et l’inflammation augmentent l’activité de l’hepcidine tandis que la carence en fer, l’hypoxie, l’érythropoïèse, et certains signaux endocrines la diminuent. Dans l’hépatocyte, la BMP6 (bone morphogenetic protein 6) semble être le ligand majeur du fer. BMP6 se lie aux récepteurs de la BMP (BMPR), entraînant la phosphorylation de molécules de signalisation intracellulaires, les SMAD. Ceux-ci sont transférés au sein du noyau pour induire la transcription de l’hepcidine. Quand les niveaux de BMP sont bas, les co-récepteurs des BMP (les protéines RGM) sont nécessaires pour induire le signal de transduction. Parmi les RGM, HJV a la plus grande affinité pour la BMP6. HJV est clivé par la matriptase-2, codée par la TMPRSS6 (transmembrane serine protease 6). Certaines mutations inactivatrices de TMPRSS6 conduisent à un excès d’hepcidine avec une anémie par carence martiale réfractaire.
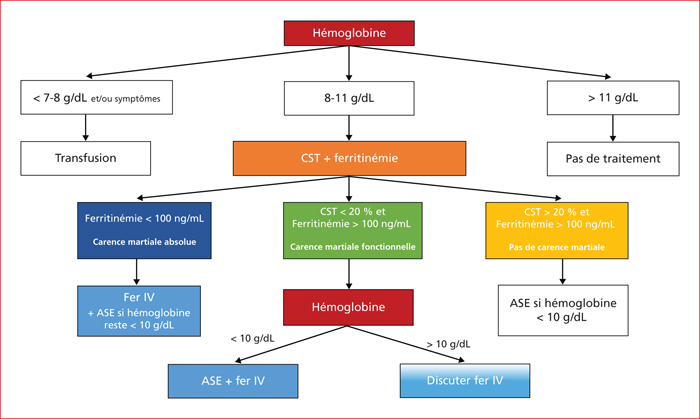
Figure 2
Diagnostic et traitement de l’anémie par carence martiale chez les patients avec un cancer traités par chimiothérapie. CST : coefficient de saturation de la transferrine ; IV : intraveineux ; ASE : agent stimulant l’érythropoïèse.

