Néphrologie & Thérapeutique
MENUUse of intravenous iron supplementation in chronic kidney disease: Interests, limits, and recommendations for a better practice Volume 11, issue 7, Décembre 2015
- Key words: Allergic reactions, Chronic kidney disease, Hemosiderosis, Intravenous iron, Iron complexes, Oral iron, Oxydative stress
- DOI : 10.1016/j.nephro.2015.04.009
- Page(s) : 531-42
- Published in: 2015
Metabolic acidosis (MAC) is a common aspect of dialysis-dependent patients. It is definitely caused by acid retention; however, the influence of other plasma ions is unclear. Understanding the mechanism of MAC and its correction is important when choosing the dialysis solution. Therefore, we assessed the relationship between intradialytic change of acid-base status and serum electrolytes.
We studied 68 patients on post-dilution hemodiafiltration, using dialysate bicarbonate concentration 32mmol/L. The acid-base disorders were evaluated by the traditional Siggaard-Anderson and modern Stewart approaches.
The mean pre-dialysis pH was 7.38, standard base excess (SBE) −1.5, undetermined anions (UA−) 7.5, sodium-chloride difference (Diff(NaCl)) 36.2mmol/L. MAC was present in 34% of patients, of which 83% had an increased UA− as a major cause of MAC. The mean nPCR was 0.99g/kg/day and correlated negatively with SBE. After dialysis, metabolic alkalosis predominated in 81%. The mean post-dialysis pH was 7.45, SBE 4, UA− 2.6, Diff(NaCl) 36.9mmol/L. ΔSBE significantly correlated with ΔUA−, but not with ΔDiff(NaCl) or ΔCl−.
MAC in patients on hemodiafiltration is mainly caused by acid retention and is associated with higher protein intake. We did not prove the effect of sodium or chloride on acid-base balance. Even though we used a relatively low concentration of dialysate bicarbonate, we recorded a high proportion of post-dialysis alkalosis caused by the excessive decrease of undetermined anions, which had been completely replaced by bicarbonate and indicated the elimination of undesirable anions, as well as of normal endogenous anions.
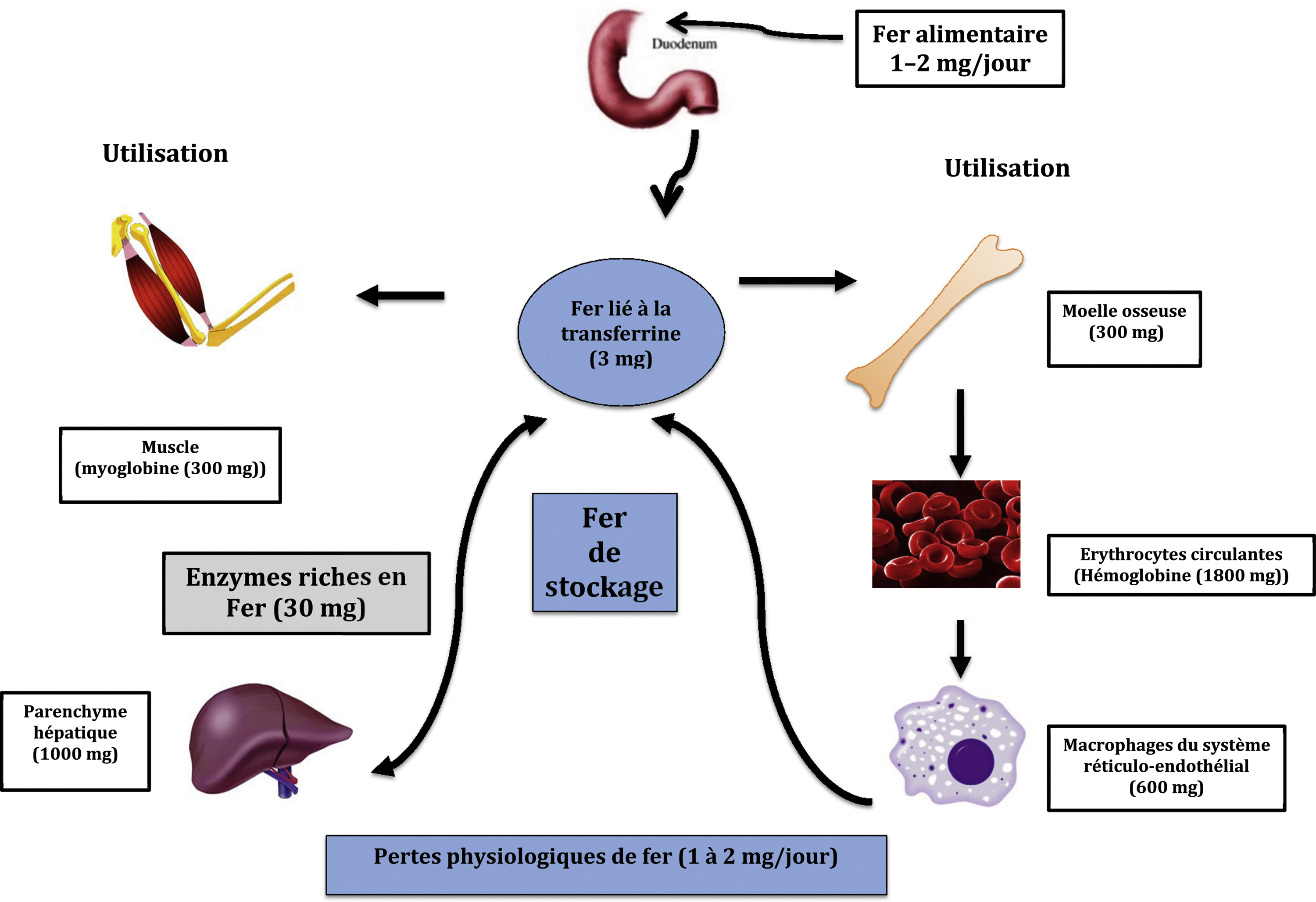
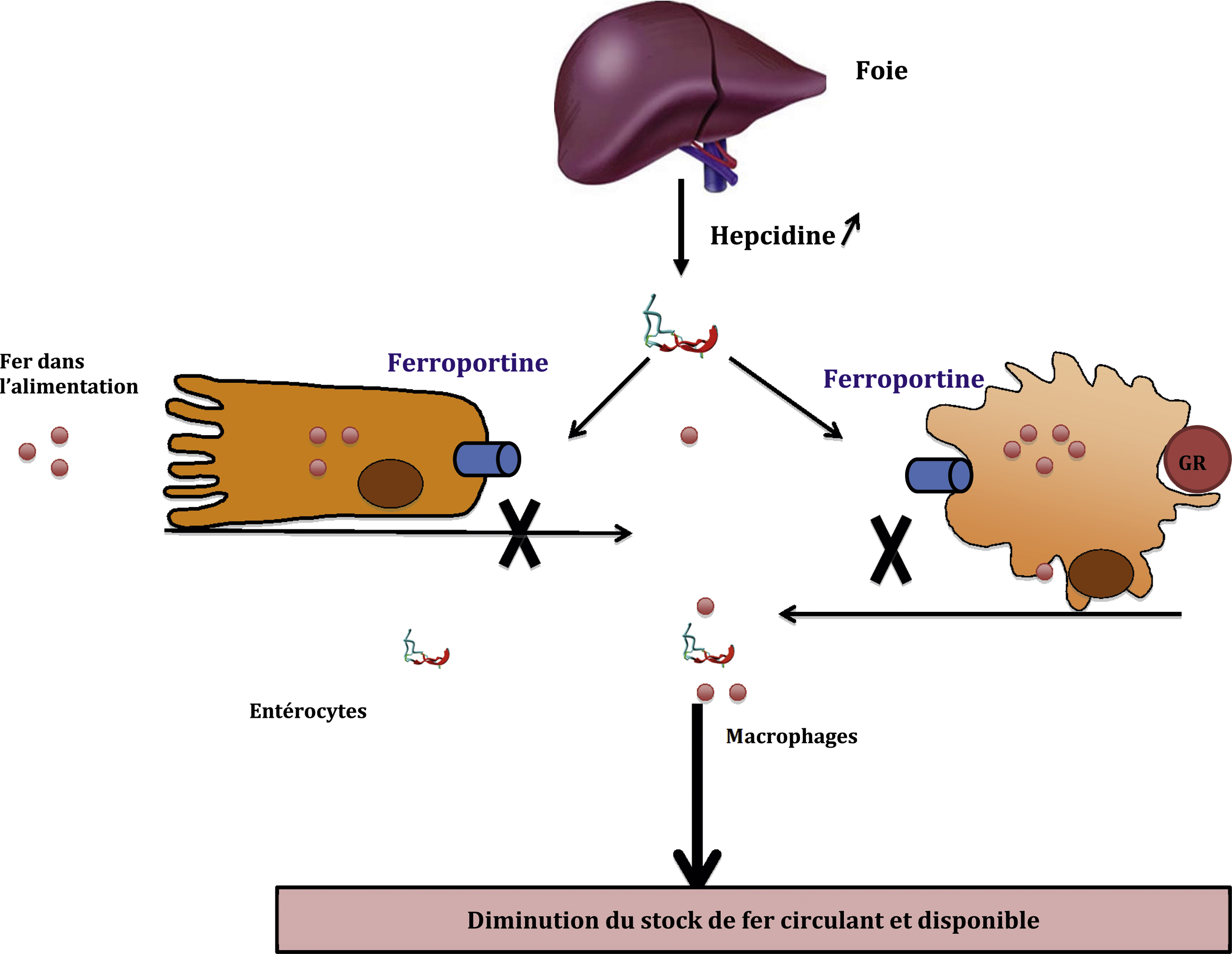
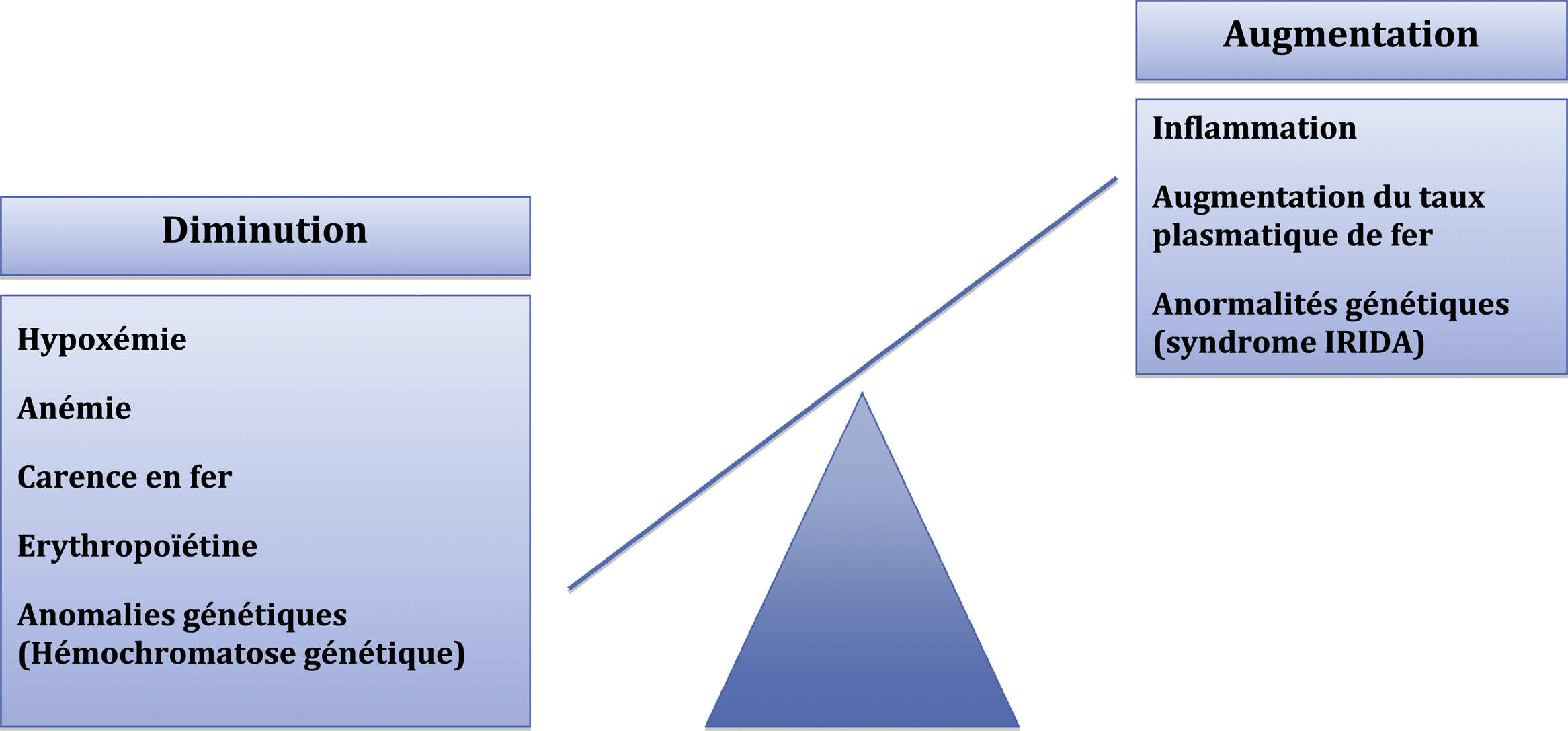
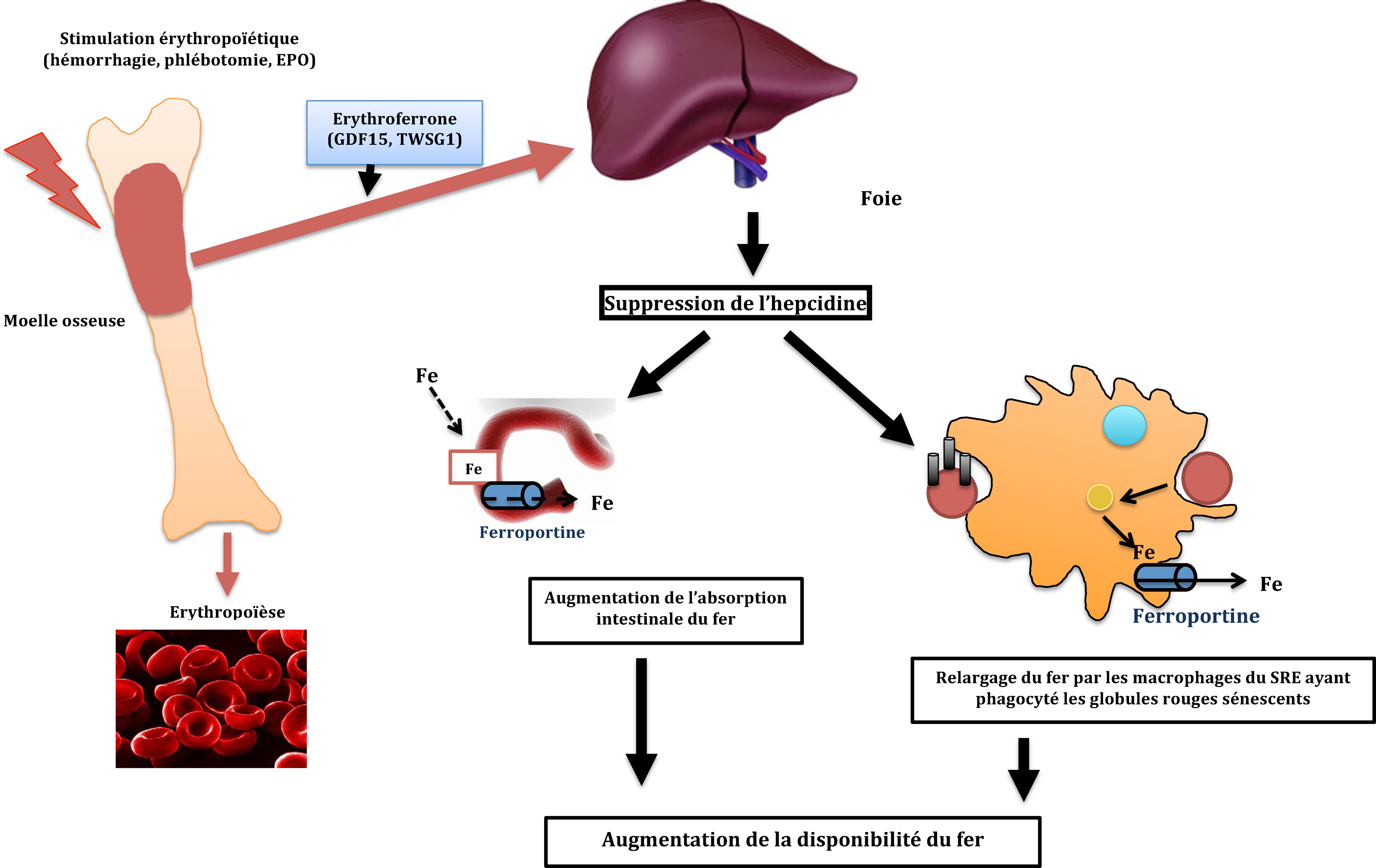
La carence en fer est un problème clinique important au cours de la maladie rénale chronique (MRC), faisant le lit de l’anémie par carence martiale et perturbant le métabolisme cellulaire dans de nombreuses réactions. La supplémentation orale, en particulier avec les sels ferreux, est souvent associée à des effets secondaires gastro-intestinaux, et de ce fait faiblement absorbée, problème qui n’est pas rencontré avec les fers injectés par voie intraveineuse. Récemment, en accord avec l’Agence européenne des médicaments, l’Agence nationale de sécurité du médicament et des produits de santé (ANSM) a renforcé le résumé des caractéristiques de toutes les spécialités à base de fer pour injection intraveineuse (IV). Les spécialités à base de fer IV ne devront être prescrites, dispensées et administrées qu’au sein des établissements de santé (publics ou privés) et une surveillance entreprise après leur perfusion. Les complexes les plus stables (dextran de bas poids moléculaire, carboxymaltose ferrique et fer isomaltoside 1000 [en cours d’agrément]) peuvent être administrés à des doses uniques plus élevées que ne le sont les autres fers sucroses (princeps et similaires). Une supplémentation en fer est recommandée chez tous les patients atteints de MRC en carence martiale, en particulier ceux qui sont anémiques et/ou reçoivent des agents stimulant l’érythropoïèse, qu’ils soient dialysés ou non. La voie intraveineuse est la voie d’administration préférée pour les patients hémodialysés, avec de nombreux essais randomisés montrant une correction de l’anémie plus rapide et plus importante que celle obtenue avec l’administration par voie orale, avec peu d’effets secondaires à court et moyen termes. Les schémas posologiques de l’autorisation de mise sur le marché (AMM) des dérivés injectables de fer devront être respectés. Chez les non-dialysés, la réponse érythropoïétique est aussi significativement meilleure par voie intraveineuse que par voie orale, avec une tolérance aussi bonne. De plus, chez les patients non dialysés, une supplémentation par voie intraveineuse de fer pourrait retarder et minimiser le besoin en agents stimulant l’érythropoïèse. En conclusion, en suivant les récentes recommandations de l’ANSM, il est désormais possible, chez les patients atteints de maladie rénale chronique, dialysée ou non, de corriger la carence martiale sans compromettre la sécurité en utilisant les différentes formes pharmaceutiques de fer, dont les préparations injectables.
Iron deficiency is an important clinical concern in chronic kidney disease (CKD), giving rise to iron-deficiency anaemia, and various impaired cellular functions. Oral supplementation, in particular with ferrous salts, is associated with a high rate of gastro-intestinal side effects and is poorly absorbed, a problem that is avoided with intravenous (IV) irons. Recently, with the approval of the European Medicines Agency's Committee for Medicinal Products for Human Use, the French Agence nationale de sécurité du médicament et des produits de santé (ANSM) took adequate measures to minimize the risk of allergic reactions, by correction on the summary of intravenous iron products characteristics. All IV iron products should be prescribed, administered and injected, inside public or private hospitals exclusively, and a clinical follow-up after the infusion for at least 30 minutes is mandatory. The most stable intravenous iron complexes (low molecular weight iron dextran, ferric carboxymaltose, and iron isomaltoside 1000 [under agreement]) can be given in higher single doses and more rapidly than less recent preparations such as iron sucrose (originator or similars). Test doses are advisable for conventional low molecular weight iron dextrans, but are no more mandatory. Iron supplementation is recommended for all CKD patients with iron-deficiency anaemia and those who receive erythropoiesis-stimulating agents, whether or not they require dialysis. Intravenous iron is the preferred route of administration in haemodialysis patients, with randomized trials showing a significantly greater increase in haemoglobin levels for intravenous versus oral iron and a low rate of treatment-related adverse events during these trials. According ANSM, physicians should apply the product's label recommendations especially the posology. In the non-dialysis CKD population, the erythropoietic response is also significantly higher using intravenous versus oral iron, and tolerability is at least as good. Moreover in some non-dialysis patients, intravenous iron supplementation might avoid or at least delay the need for erythropoiesis-stimulating agents. Following the new ANSM's recommendations, we now have the ability to achieve iron stores replenishment correctly and conveniently in dialysis dependent and non-dialysis dependent CKD patients without compromising safety using the various pharmaceutical forms of iron products especially intravenous compounds.