Néphrologie & Thérapeutique
MENUShort-term effects with sucroferric oxyhydroxide in hemodialysis patients: Experience in NephroCare France Volume 15, issue 1, Mars 2019
- Key words: Calcium-free phosphate binder, Dialysis, Hyperphosphatemia, Real-world evidence, Sucroferric oxyhydroxyde
- DOI : 10.1016/j.nephro.2018.08.003
- Page(s) : 29-34
- Published in: 2019
Malgré une amélioration de la prise en charge de l’hyperphosphatémie des patients hémodialysés au cours des dernières années, une importante proportion d’entre eux reste insuffisamment traitée et donc exposée aux complications osseuses et cardiovasculaires auxquelles elle est associée. L’intérêt des chélateurs non calciques dans l’arsenal thérapeutique se confirme puisqu’ils permettent de réduire significativement la phosphatémie, tout en permettant de limiter la charge en calcium. À ce jour, l’oxyhydroxyde sucroferrique (OHS) est le seul chélateur non calcique à base de fer disponible en France.
Une cohorte de patients traités par OHS a été extraite à partir de la base de données EUCLID 5 entre juin 2016 et décembre 2017 et les effets sur les paramètres du métabolisme minéral et la ferritine ont été analysés de façon rétrospective.
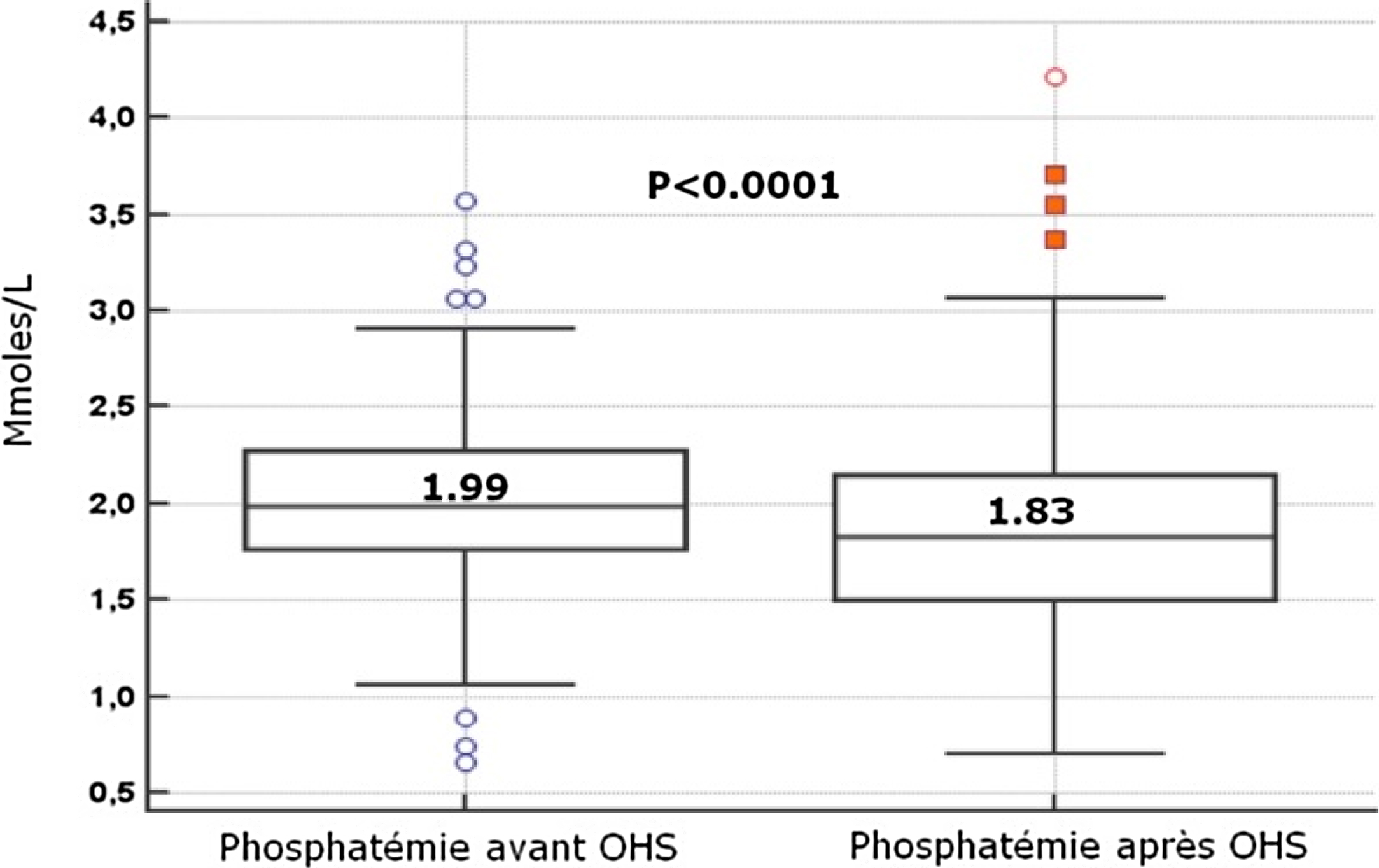
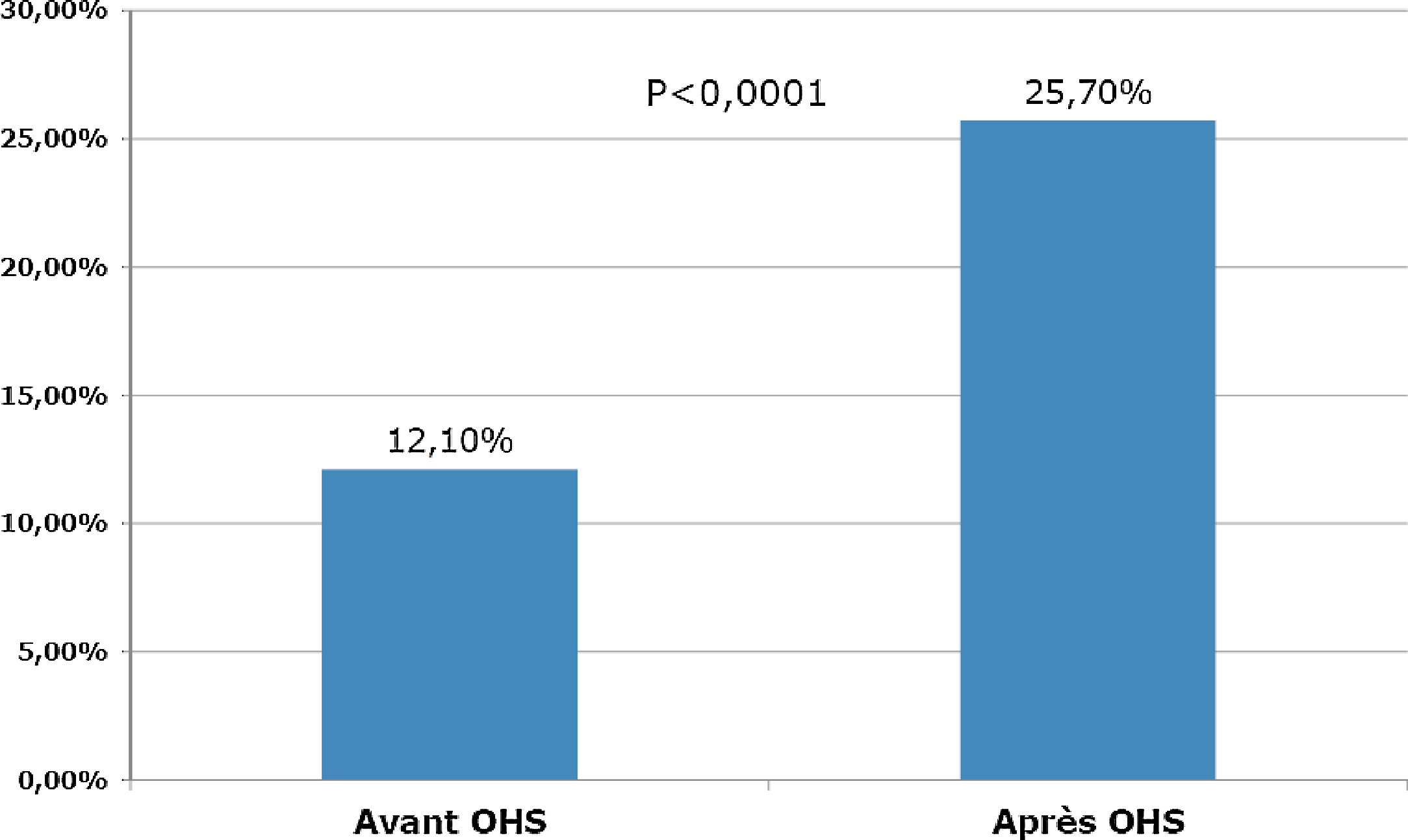
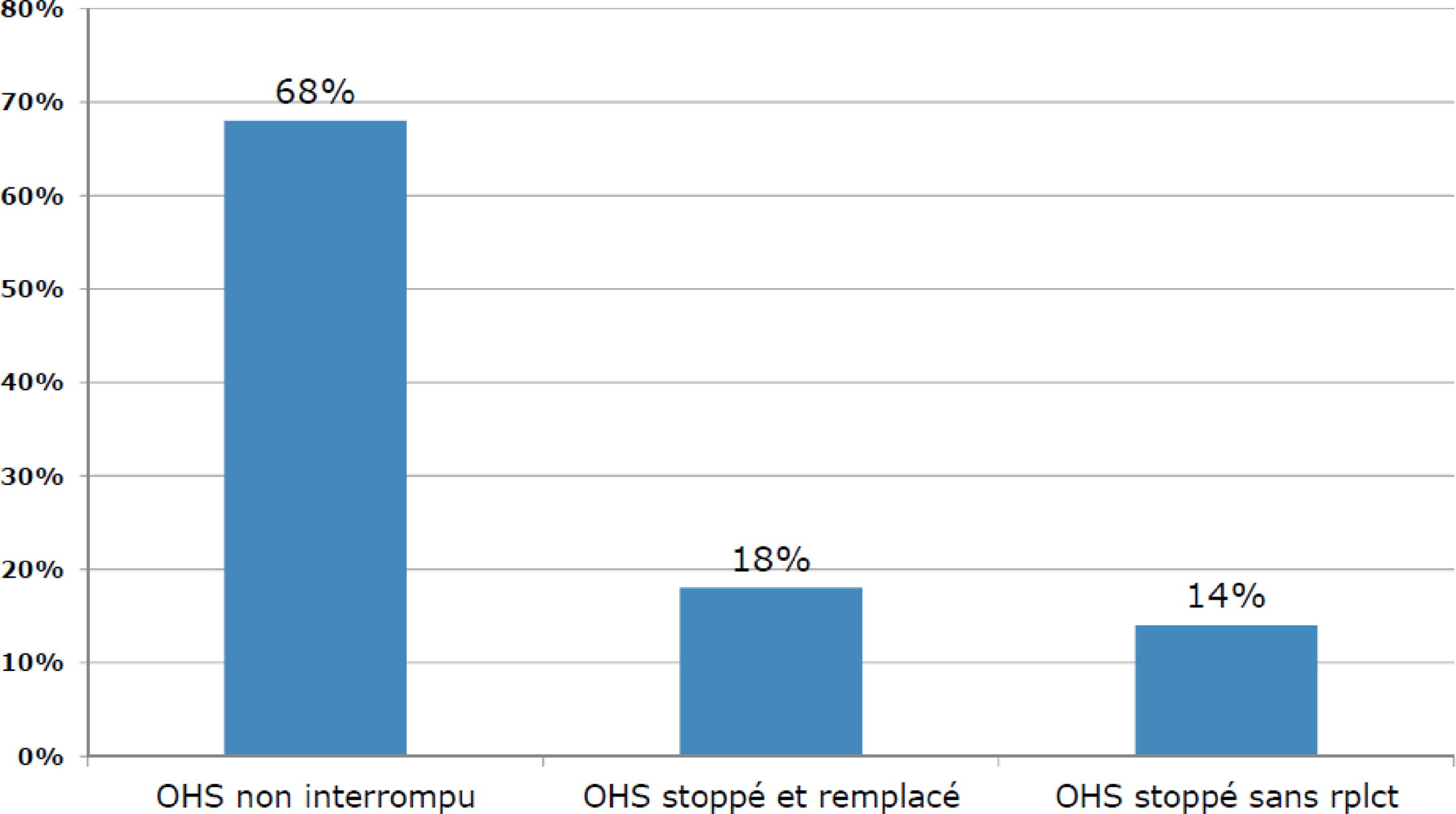
Deux cent soixante-deux patients avec une prescription d’OHS ont été identifiés. La médiane de durée de traitement a été de 4,3 mois (1,84–10,99). La phosphatémie moyenne de milieu de semaine a baissé de façon significative deux mois avant et après mise sous OHS (1,99 à 1,83 mmol/L ; p<0,0001) avec une augmentation de 12,1 à 25,7 % (p<0,0001) de patients dans la cible de phosphates (1,5 mmol/L), sans modification de la calcémie et de la parathormone. La ferritinémie moyenne a augmenté significativement de 362 à 427 μg/L en 3 mois (p=0,0049). Le traitement a été interrompu et remplacé chez 18 % des patients. Le nombre de comprimés et les effets secondaires n’ont pas pu être analysés à partir de la base EUCLID 5.
Dans la cohorte NephroCare, le traitement par OHS a été efficace sur la phosphatémie en doublant le pourcentage de patients dans la cible. Il n’y a pas eu d’effets à court terme sur la calcémie et la parathormone. L’augmentation modérée de la ferritine confirme l’analyse de l’étude de phase III et son extension. Le risque de surcharge en fer et l’effet sur la gestion de l’anémie en termes d’épargne d’EPO sont actuellement en cours d’étude.
L’OHS est une nouvelle alternative efficace aux chélateurs non calciques. Une meilleure connaissance de l’OHS et de ses effets secondaires par les praticiens et les patients pourra permettre d’optimiser la prise en charge de l’hyperphosphatémie des patients dialysés. La majoration de la ferritine apparaît comme un épiphénomène au milieu des besoins importants en fer et de la surveillance régulière du traitement de l’anémie.
Despite a better management of hyperphosphatemia in haemodialysis patients observed during the past years, most of them remain insufficiently treated and exposed to bone and cardiovascular complications that are associated with this biological abnormality. The availability of calcium-free phosphate binders among therapeutical options is confirmed to significantly reduce serum phosphate levels without the risk of excess exposure to calcium. Currently sucroferric oxyhydroxyde (SO) is the only iron-based phosphate binder available in France.
A cohort of patients prescribed OHS has been extracted from the EUCLID 5 database between June 2016 and December 2017. The effects on bone mineral metabolism and ferritin have been retrospectively studied.
Two hundred and sixty-two patients with OHS prescription have been identified. The OHS treatment duration median was 4.3 months (1.84–10.99). The average midweek phosphatemia decreased significantly after OHS prescription (from 1.99 to 1.83 mmol/L ; P<0.0001) with a significant increase of the proportion of patients (12.1 to 25.7% ; P<0.0001) reaching the phosphate target of 1.5 mmol/L, without significant change in calcemia and PTH. Ferritinemia significantly increased from 362 to 427 μg/L in 3 months (P=0.0049). OHS therapy has been stopped and replaced in 18% of the cases.
Among the NephroCare cohort, OHS therapy was efficient to decrease phosphatemia and to increase significantly the proportion of patients in target. There were no short term changes in calcemia and PTH. The slight increase in ferritin confirms the findings of the phase III study and its extension. The effects on the pills count and the OHS side-effects are analyzed from literature. The risk of iron overload and the impact on the anemia management including EPO sparing are currently under study.
OHS therapy appears to be a new efficient alternative to non-calcium phosphate binders. A better knowledge of its side effects will help the patients and the physician to optimize the phosphate balance management. The slight increase in ferritin can be considered as an epiphenomenon because of the important iron needs and frequent check of this parameter in the anemia management.