Néphrologie & Thérapeutique
MENUAA amyloidosis Volume 13, issue 4, Juin 2017
- Key words: AA amyloidosis, Immunohistochemistry, Nephropathy, Serum amyloid A protein
- DOI : 10.1016/j.nephro.2017.03.001
- Page(s) : 258-64
- Published in: 2017
Central retinal vein occlusion (CRVO) is one of the most common retinal vascular disease. Macular edema associated is responsible of the major decrease in visual acuity. The main causes often implicated are high blood pressure and diabetes. Other etiologies should be sought including CRVO secondary to antiphospholipid syndrome (APS). This rare etiology is associated with a poor prognosis when late diagnosed. Owing to the high associated mortality, early diagnosis and prompt treatment are necessary. We describe a case of APS complicated by a catastrophic antiphospholipid syndrome in a patient who presented a decrease visual acuity.
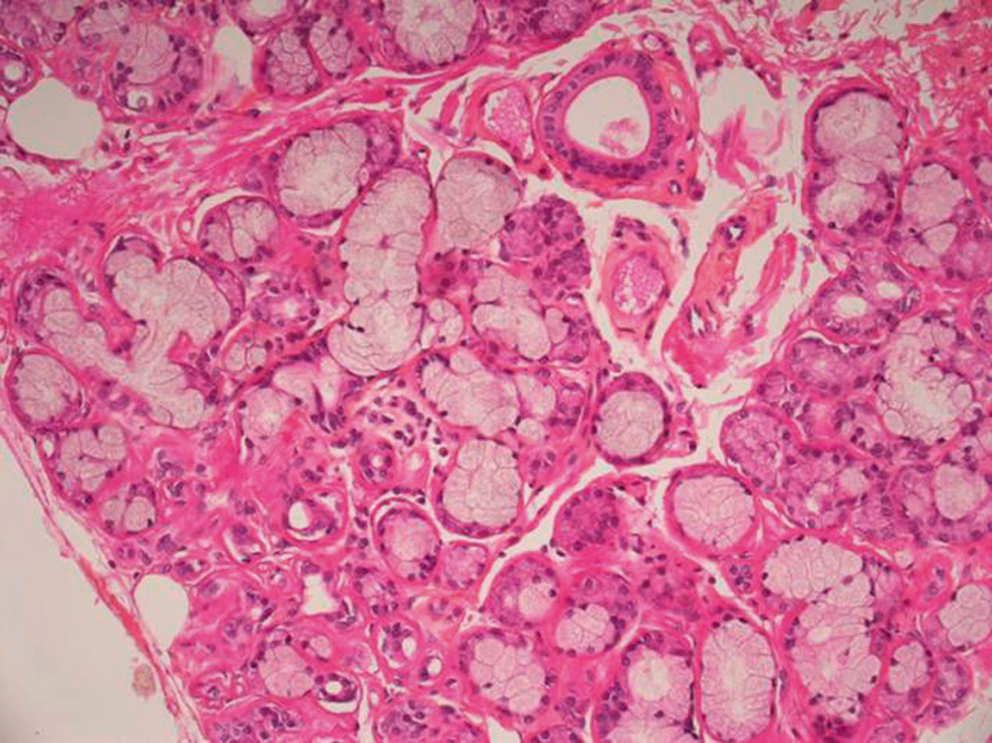
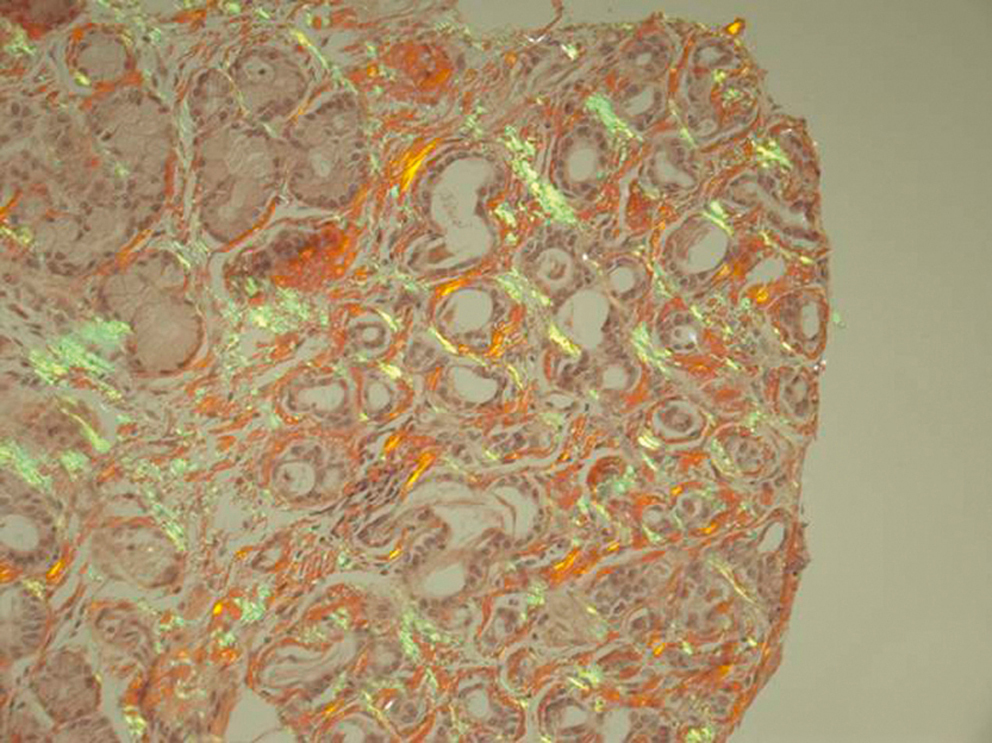
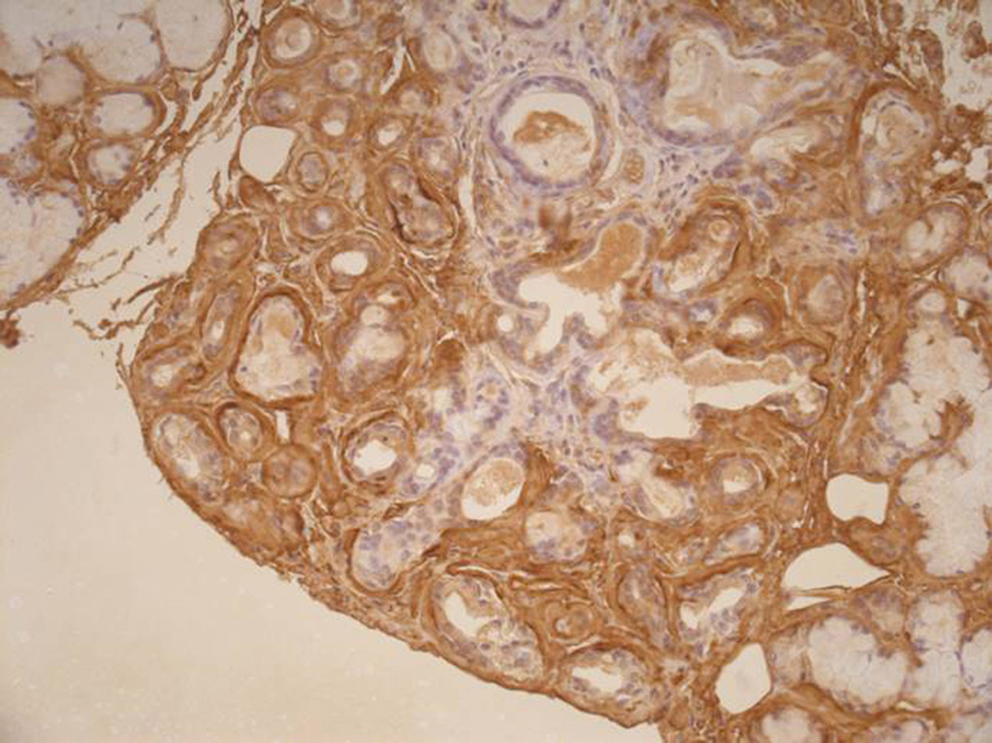
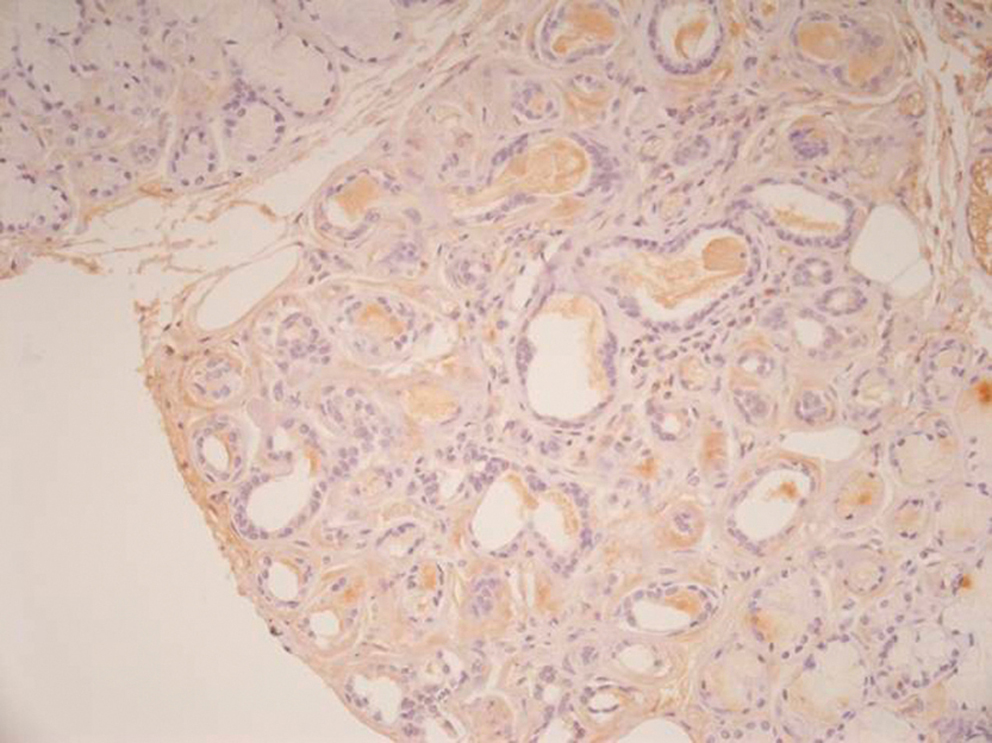
L’amylose AA reste l’une des trois grandes variétés d’amylose multisystémique, avec l’amylose AL et les formes héréditaires. Son incidence semble toutefois diminuer dans les pays occidentaux, où les maladies inflammatoires sont la principale cause d’amylose, au premier rang desquelles se tient la polyarthrite rhumatoïde, suivie par la spondylarthrite ankylosante et les syndromes auto-inflammatoires. Parmi les tumeurs, il faut signaler la maladie de Castleman, dont l’ablation chirurgicale permet parfois la résolution des symptômes de l’amylose. Une inflammation prolongée est un prérequis au développement d’une amylose AA ; la protéine majoritaire des dépôts est un fragment de la protéine serum amyloid A (SAA), l’une des protéines de la réaction inflammatoire. Cependant, d’autres facteurs, notamment génétiques, sont impliqués dans la susceptibilité à la survenue de l’amylose AA. La néphropathie est la principale manifestation clinique de l’amylose de type AA. La recherche de protéinurie et la mesure de la créatinine plasmatique restent les éléments de dépistage de l’amylose au cours de toute maladie qui comporte une inflammation chronique. Le diagnostic précis de l’amylose AA nécessite de confronter l’ensemble des données cliniques et histologiques et notamment de l’immunohistochimie, afin de ne pas la confondre avec l’une des autres variétés. Une fois installée, l’amylose AA reste de mauvais pronostic en raison de l’insuffisance rénale terminale, qui est le terme ultime de la néphropathie, et de l’atteinte digestive qui s’accompagne de dénutrition profonde. Les traitements actuels sont ciblés sur la maîtrise de l’inflammation ; des médicaments inhibant l’interaction de la protéine AA aux composants communs de l’amylose (composant amyloïde P et héparane sulfate) sont en cours d’évaluation.
AA amyloidosis remains one of the three main types of systemic amyloidosis with AL and ATTR. Its incidence has been however decreasing recently in Western countries. Chronic inflammatory diseases are currently the first cause of AA amyloidosis, including rheumatoid arthritis, spondyloarthritis and autoinflammatory diseases. Castleman's disease is a specific cause of AA amyloidosis that can be cured by surgery. A chronic inflammatory response is required to develop amyloidosis. Other genetic and environmental factors are also involved. The first clinical manifestation is a chronic glomerular nephropathy, which can be detected by urine examination and serum creatinine measure. Immunohistochemistry is mandatory to confirm the clinical diagnosis of AA amyloidosis and to avoid misdiagnosis. Long-term prognosis remains poor on chronic dialysis in case of clinical gut involvement. Current treatment is based on the control of the inflammatory response. Specific treatment aimed at inhibiting amyloid formation targeting serum amyloid P component and heparan sulphate are currently evaluated.