Médecine thérapeutique
MENUUn cœur foudroyé Volume 24, issue 2, Mars-Avril 2018
Figures
La foudre est un phénomène naturel de décharge électrostatique ; quoique assez fréquent, il est rarement responsable d’accident chez l’homme. La foudre blesse 240 000 personnes et en tue 20 000 par an dans le monde ; la mortalité mondiale liée au foudroiement varie ainsi de 0,2 à 1,7 par million d’habitants par an [1]. Les conséquences de l’agression électrothermique liée à la foudre sont très polymorphes, allant de lésions cutanées bénignes au décès immédiat. Cette morbimortalité est essentiellement associée aux effets cardiaques de la foudre : dépolarisation cardiaque et asystolie, arythmies bénignes ou létales, dysfonctionnement d’implants cardiaques, ischémie cardiaque, lésions myocardiques et aortiques [2]. La prise en charge et la surveillance de ces patients « hors normes » imposent une vigilance et une expertise particulières. Cet article discute le cas d’une myocardite associée à un foudroiement, à la lumière des données de la littérature.
Observation
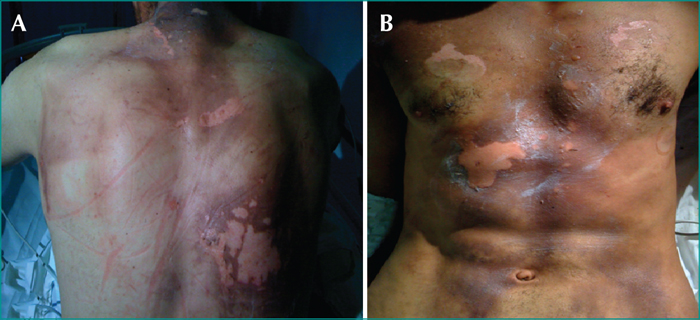
Un jeune patient de 32 ans, agriculteur de profession, sans antécédents pathologiques notables, a été victime d’un foudroiement sur son champ de travail. Le transport aux urgences était immédiat mais non médicalisé. À son admission aux urgences, le patient était conscient, légèrement agité, sans souvenirs précis de l’accident. L’examen clinique trouvait un patient polypnéique, à 34 cycles par minute, avec une SpO2 à 73 % à l’air ambiant. Il était tachycarde à 134 battements par minute, hypotendu à 79/40 mmHg avec des extrémités froides et des marbrures généralisées. L’auscultation des deux champs pulmonaires objectivait des râles crépitants diffus. Il présentait par ailleurs une brûlure cutanée étendue à environ 20 % de la surface corporelle, intéressant la face antérieure du thorax, le dos et la région sacrée, à prédominance de deuxième degré profond (figure 1). L’électrocardiogramme (ECG) montrait une tachycardie sinusale avec un sous-décalage diffus du segment ST. Les anomalies du bilan biologique étaient : une troponine Ic élevée à 4,75 μg/L (seuil à 0,1 μg/L), une légère rhabdomyolyse et une hyperlactatémie. À la gazométrie artérielle, on notait une hypoxémie avec un rapport PaO2/FiO2 à 270 et une acidose métabolique. Les fonctions rénale et hépatique étaient normales. La radiographie thoracique était suggestive d’un œdème pulmonaire.
Le patient a rapidement été mis en condition : position demi-assise, abord veineux, oxygénothérapie au masque à haute concentration puis ventilation non invasive en pression positive, furosémide intraveineux et réhydratation intraveineuse prudente. À l’échocardiographie, on notait :
- –une dysfonction ventriculaire gauche systolodiastolique avec un ventricule gauche dilaté, une hypokinésie globale sans anomalie de la cinétique segmentaire avec une fraction d’éjection ventriculaire gauche (FEVG) estimée à 30 % (normale > 55 %) et une augmentation des pressions de remplissage,
- –une hypertension artérielle pulmonaire importante, à 55 mmHg, sans dysfonction droite ni épanchement péricardique ni dissection de la portion initiale de l’aorte ascendante.
Devant les données échocardiographiques et les signes clinicobiologiques de bas débit cardiaque, la dobutamine fut introduite à la dose de 10 gamma/kg/min. L’évolution était marquée par une stabilisation hémodynamique et respiratoire : amélioration de la pression artérielle et de la diurèse horaire, disparition des marbrures et de l’agitation, normalisation du taux de lactates artériel, diminution des râles crépitants et évolution favorable de la cinétique des enzymes cardiaques. Un scanner cérébral ainsi qu’un examen somatique plus approfondi à la recherche de lésions méconnues (notamment auditives, oculaires et neurologiques périphériques) ont été réalisés après stabilisation initiale et n’ont décelé aucune anomalie.
Le sevrage de la dobutamine était progressif sur 72 h, et le patient était mis sous traitement cardiologique anti-ischémique de base : aspirine, statine, bêtabloquant et inihibiteur de l’enzyme de conversion. Le contrôle échocardiographique objectivait une amélioration de l’éjection ventriculaire gauche à partir du troisième jour puis une normalisation à trois semaines. Le patient a par ailleurs bénéficié de soins quotidiens pour ses brûlures et d’un soutien psychologique.
Discussion
Le foudroiement représente l’électrisation par courant de foudre, phénomène naturel lié à un transfert d’énergie entre un nuage chargé négativement et un conducteur terrestre de charge opposée.
Le foudroyé est généralement un jeune homme en bonne santé, victime dans un contexte d’accident isolé, rarement collectif, se produisant en plein air au cours d’activités sportives, de loisirs ou professionnelles (agriculteurs et ouvriers de chantier) [3]. Notre patient était un jeune agriculteur, seul foudroyé sur son site de travail en présence de témoins.
La foudre, courant électrique continu massif de très haute tension et de très brève durée, agit sur le corps humain soit directement, par contact ou par éclair, soit indirectement, via un conducteur. Les accidents d’exposition échappent à toute description précise du fait de la complexité des mécanismes en cause : électrothermiques, blast, acoustiques, lumineux et traumatismes indirects [3]. Le tableau lésionnel peut être polymorphe et multisystémique, mais il est dominé par l’arrêt cardiaque, cause immédiate de décès, et les dégâts neurologiques centraux et périphériques, sources de séquelles invalidantes chez les survivants [4].
En cas de coup de foudre direct, le trajet du courant est souvent longitudinal entre la tête et les membres inférieurs intéressant le cerveau et le cœur. Les lésions cardio-vasculaires sont ainsi fréquentes, diverses et de plus en plus détaillées dans la littérature [5]. L’atteinte myocardique directe dominait le tableau clinique de notre patient indemne de toute atteinte neurologique. Les modifications myocardiques sont électriques et/ou mécaniques et peuvent conduire à un arrêt cardiocirculatoire. Ce dernier surviendrait le plus souvent en asystolie qu’en fibrillation ventriculaire, la décharge de foudre entraînant une dépolarisation brutale de l’ensemble des cellules myocardiques (asystolie) parfois suivie d’une reprise spontanée de l’automatisme cardiaque [6]. La sidération des centres respiratoires lors du passage du courant ou les lésions cérébrales graves, secondaires aux traumatismes par chute violente ou par projection, peuvent être tout aussi létales [3]. La réanimation cardiopulmonaire de base pratiquée sur les lieux de l’accident pourrait améliorer le pronostic. Le transport de notre patient était non médicalisé et aucun des témoins n’était formé aux gestes de secourisme. Heureusement, le recours à une réanimation cardiopulmonaire de base sur les lieux de l’accident et lors du transport n’était pas nécessaire. La lésion cardiaque est multifactorielle : spasme et thrombose des artères coronaires fragilisées par le courant, décharge catécholaminergique induite par le stress avec production de radicaux libres, effet Joule responsable de nécroses plus ou moins étendues [5]. Les modifications électriques peuvent être précoces ou apparaître secondairement, et être fatales ou réversibles en quelques jours. Un ECG initial est systématique et doit être répété, même chez les victimes asymptomatiques. Il permet d’objectiver des troubles du rythme cardiaque (tachycardie sinusale, arythmies auriculaires ou extrasystoles), des troubles de repolarisation (modifications non significatives du segment ST et de l’onde T, allongement temporaire de l’intervalle Q) ainsi que des dysfonctions d’implants cardiaques [7]. L’ECG de notre patient notait une tachycardie sinusale avec un sous-décalage non significatif de ST, et s’est normalisé au bout de trois semaines. L’atteinte mécanique cardiaque comprend quant à elle : sidération myocardique et myocardite, ischémie et infarctus du myocarde, contusions myocardiques et lésions péricardiques ainsi que des lésions aortiques disséquantes [5]. Des anomalies échocardiographiques particulières ont également été observées chez les victimes de foudroiement direct. Hayashi met ainsi en évidence un anévrisme apical appelé takotsubo-shaped hypokinesis du ventricule gauche sans anormalités valvulaires apparentes [8]. Du point de vue biologique, les lésions myocardiques objectivées par une élévation des enzymes cardiaques sont quasi constantes en cas de foudroiement direct [8]. Notre patient s’est présenté dans un tableau de choc cardiogénique avec défaillance ventriculaire gauche nécessitant le recours à une ventilation non invasive en pression positive et un support inotrope. L’échocardiographie objectivait une hypokinésie globale sans dyskinésie segmentaire associée à une cinétique dégressive des enzymes cardiaques, ce qui concordait avec une atteinte myocardique directe. L’exploration coronaire n’était pas indiquée. La récupération d’une sidération myocardique se fait en général au bout de un mois selon l’étude de Lichtenberg et al.[2]. Elle était de trois semaines dans notre cas.
Un foudroyé est sûrement un électrisé et probablement un traumatisé, un brûlé ou un « blasté ». Sa prise en charge, multidisciplinaire et précoce, rejoint celle du traumatisé grave. Les mesures de réanimation cardiocirculatoire, respiratoire et hydroélectrolytique ainsi que la prévention de l’hypothermie doivent être initiées rapidement. L’hospitalisation est obligatoire. Le monitorage hémodynamique doit être adapté. L’ECG, la troponine et l’échocardiographie dans le cadre du FAST (focused assessment sonography for trauma) sont systématiques. La prise en charge cardiovasculaire rejoint le traitement cardiologique traditionnel. La surveillance neurologique est nécessaire, avec réalisation d’une imagerie cérébrale au moindre signe d’appel. Examen oculaire et otoscopique, prophylaxie antitétanique, soins des brûlures, aponévrotomies de décharge peuvent être indispensables. Un suivi à long terme doit être assuré pour détecter les atteintes à expression tardives et un soutien psychologique pour une réhabilitation socioprofessionnelle est souhaitable [9].
Conclusion
L’atteinte myocardite liée au foudroiement est complexe et multifactorielle. L’évaluation minimale du cœur foudroyé nécessite un monitorage rapproché de l’ECG et de l’échocardiographie ainsi que de la troponine. Une prise en charge précoce et agressive constitue un facteur pronostique pouvant améliorer le devenir de ces patients considérés comme traumatisés graves.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt en rapport avec cet article.
![]() This work is licensed under a
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License
This work is licensed under a
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License