Hépato-Gastro & Oncologie Digestive
MENUNew standards and personalised approaches in cholangiocarcinoma Volume 26, supplement 6, Décembre 2019
Épidémiologie des cancers des voies biliaires
Des tumeurs hétérogènes et rares
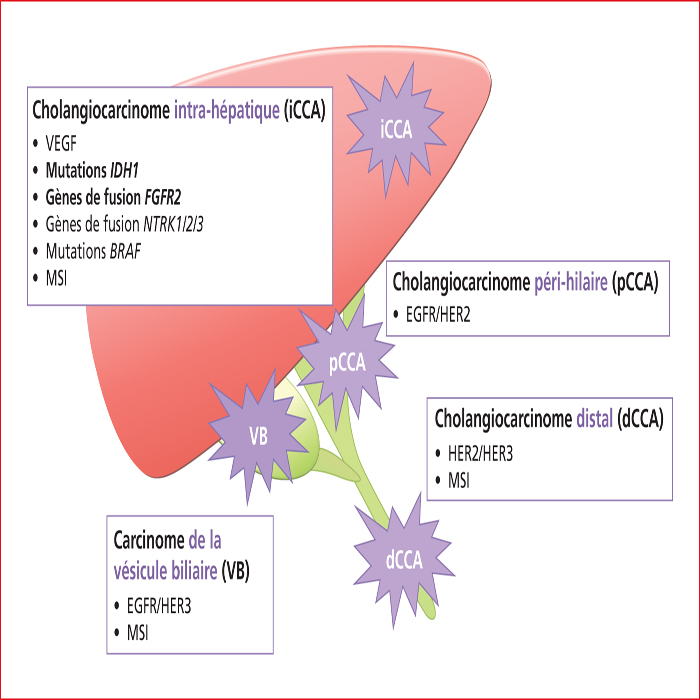
Les cancers des voies biliaires (CVB) sont un groupe hétérogène d’adénocarcinomes développés à partir de l’épithélium des voies biliaires. Ils représentent la deuxième tumeur primitive du foie termes d’incidence après le carcinome hépatocellulaire (CHC) [1]. La localisation anatomique permet d’en distinguer quatre sous-types : (1) les cholangiocarcinomes (CCA) intra-hépatiques ou périphériques, développés au sein du parenchyme hépatique ; (2) les CCA péri-hilaires ou extra-hépatiques proximaux, entre les canaux biliaires de second ordre et le canal cystique, comprenant les tumeurs de Klatskin ; (3) les CCA extra-hépatiques distaux, siégeant au niveau de la voie biliaire principale en dessous de la bifurcation du canal cystique ; et (4) les adénocarcinomes de la vésicule biliaire [1]. Les CCA représentent la majorité des CVB (80 %-82 % des formes localisées et 60 %-72 % des formes avancées).
Les CVB sont des tumeurs rares, avec une incidence < 6/100 000, soit environ 2 000 à 3 000 nouveaux cas par an en France [1]. Cette incidence, variable dans le monde (supérieure en Asie), est en augmentation, principalement pour les CCA intra-hépatiques [1, 2]. Les principaux facteurs de risque sont les maladies inflammatoires chroniques des voies biliaires, les parasitoses (douves en Asie), la consommation d’alcool, les infections par les virus des hépatites B et C, le syndrome métabolique et surtout la présence d’une cirrhose (risque relatif : 20) [1, 2]. Le pronostic des CVB est sombre, avec un taux de survie globale (SG) à cinq ans inférieur à 20 %, en raison (i) d’un diagnostic souvent tardif, à un stade avancé (dans 70 % des cas), du fait de symptômes initiaux non ou peu spécifiques, et (ii) de récidives post-opératoires fréquentes [1]. Les cancers des voies biliaires sont un groupe hétérogène d’adénocarcinomes développés à partir de l’épithélium des voies biliaires
Un challenge diagnostique
Le diagnostic de CCA, en particulier intra-hépatique, peut être difficile à l’imagerie. Les deux principaux diagnostics différentiels sont les CHC et les métastases d’adénocarcinomes de primitif « inconnu » (ACUP) [3].
Les CHC représentent 90 % des tumeurs malignes primitives du foie et se développent le plus souvent sur une hépatopathie chronique sous-jacente. Les CCA intra-hépatiques se développent quant à eux le plus souvent sur foie non-cirrhotique, mais affectent aussi les patients cirrhotiques, et peuvent présenter la même apparence en imagerie, justifiant le recours large à la biopsie tumorale chez ces patients [4]. Il existe par ailleurs des formes de chevauchement entre ces deux types de tumeurs (hépatocholangiocarcinome).
Les CVB sont par ailleurs fréquemment confondus avec des métastases de primitifs extra-hépatiques : la réalisation d’un profil moléculaire sur 252 ACUP permettait de reclasser 21 % d’entre eux en CVB, représentant l’origine la plus fréquente de ces lésions [5] ; la relecture de l’imagerie de 150 ACUP révélait que 12 % étaient compatibles avec un CCA intra-hépatique avec notamment un aspect de rétraction capsulaire typique (données non publiées, J. Valle). Le diagnostic de cholangiocarcinome, en particulier intra-hépatique, peut être difficile à l’imagerie
Traitements des formes localisées
Chirurgie
Seulement 20 %-30 % des CCA sont résécables au moment du diagnostic, la non-résécabilité étant liée à la présence de localisations à distance, à une atteinte vasculaire, et/ou à l’importance de l’envahissement hépatique ne permettant pas de conserver un volume suffisant de parenchyme hépatique sain [2].
La résection chirurgicale, seul traitement qui permette une survie prolongée, doit être envisagée chaque fois que possible, et discutée au sein d’une équipe multidisciplinaire expérimentée en chirurgie hépato-biliaire [1]. L’objectif de la chirurgie est d’obtenir la résection complète (marges R0) de la tumeur et un curage ganglionnaire [1].
La sélection des patients pour la chirurgie est essentielle et basée sur l’analyse minutieuse des imageries pré-opératoires (IRM hépatique avec cholangio-IRM, scanner thoraco-abdomino-pelvien injecté) et l’évaluation de l’opérabilité (âge, état général, co-morbidités) [1].
La chirurgie présente des particularités selon la localisation de la tumeur primitive (intra-hépatique, extra-hépatique, vésicule biliaire). La morbidité et la mortalité des hépatectomies majeures peuvent être améliorées par le drainage biliaire pré-opératoire du futur foie restant en cas d’ictère puis, le cas échéant, l’embolisation portale pré-opératoire du foie à réséquer afin d’hypertrophier le futur foie restant si le volume de celui-ci est insuffisant à la volumétrie tomodensitométrique (< 30 % en l’absence de cirrhose, < 40 % en cas de cirrhose) [1]. Le drainage biliaire peut être complexe et doit être réalisé au sein d’équipes expérimentées.
L’envahissement microscopique des marges de résection (statut R1) (SG à cinq ans < 10 %), l’envahissement ganglionnaire (SG à 5 ans < 5%) et vasculaire sont les principaux facteurs de mauvais pronostic, ainsi que la taille tumorale, la multifocalité pour les CCA intra-hépatiques et le grade de différenciation [6].
Les récidives post-opératoires sont fréquentes et la SG à cinq ans des patients opérés ne dépasse pas 25 %-35 % [2]. Ces résultats ont conduit à poser la question de l’intérêt des traitements péri-opératoires. La résection chirurgicale doit être envisagée chaque fois que possible et discutée au sein d’une équipe multidisciplinaire expérimentée en chirurgie hépato-biliaire
Traitement néo-adjuvant
Un traitement néo-adjuvant est fréquemment impossible chez ces patients du fait de l’ictère et/ou de l’altération de l’état général. Il n’existe pas de données issues d’essais prospectifs randomisés permettant de recommander la réalisation d’un traitement néo-adjuvant (chimiothérapie et/ou radiothérapie pré-opératoire) [1]. Un protocole de radiochimiothérapie (RCT) suivie de transplantation hépatique a été établi par la Mayo Clinic pour les patients ayant un CCA péri-hilaire, mais n’est pas devenu un standard thérapeutique [7] ; cette stratégie multidisciplinaire est en cours d’évaluation versus une approche chirurgicale classique dans une étude de phase III (étude TRANSPHIL, NCT02232932).
Traitement adjuvant
Jusqu’en 2017, le niveau de preuve était trop faible pour recommander de façon systématique un traitement adjuvant chez les patients opérés d’un CVB [1] ; la plupart des centres proposaient une chimiothérapie adjuvante, en particulier en cas de résection R1 ou d’envahissement ganglionnaire, sur la base d’un faible niveau de preuve [8, 9]. L’étude française de phase III PRODIGE 12-ACCORD 18, qui comparait six mois de chimiothérapie adjuvante par GEMOX (gemcitabine et oxaliplatine) à la surveillance, s’est révélée négative pour son objectif principal (survie sans récidive [SSR]) [10]. En revanche, l’étude anglaise de phase III BILCAP, qui évaluait une chimiothérapie adjuvante par capécitabine (selon un schéma classique de 1 250 mg/m2, deux fois par jour, 14 jours sur 21, pendant six mois) versus surveillance, bien que négative pour son objectif principal (SG sur la population en intention de traiter : 51,1 vs. 36,4 mois, Hazard Ratio [HR] = 0,81, p = 0,097), a montré une amélioration significative de la SG dans la population per protocole (HR = 0,75, p = 0,028) et après ajustement sur le sexe, grade et statut ganglionnaire (HR = 0,71, p < 0,01), et de la SSR avec la capécitabine [11]. Malgré la non-significativité de l’étude, en raison d’un gain de survie de 15 mois et d’un profil de tolérance favorable, le traitement adjuvant par capécitabine pour six mois est considéré comme un nouveau standard. Le traitement adjuvant par capécitabine pour six mois est considéré comme un nouveau standard
Tumeurs localement avancées à prédominance hépatique : place des traitements locorégionaux
Si les CCA extra-hépatiques sont anatomiquement et biologiquement proches des cancers du pancréas, et sont classiquement des tumeurs peu vascularisées, les CCA intra-hépatiques, à l’inverse, ont la particularité d’être des tumeurs souvent hypervasculaires au temps artériel [12]. Les traitements intra-artériels hépatiques (chimiothérapie, radioembolisation à l’Yttrium-90, chimioembolisation intra-artérielle hépatique conventionnelle, et embolisation sélective par micro-billes chargées de chimiothérapie) ont été étudiés pour le traitement des CCA intra-hépatiques localement avancés (non résécables, non métastatiques) dans certains centres [13]. Les effets de la radiothérapie interne sélective avec des microsphères d’Yttrium-90 ont été analysés dans une revue systématique de 12 études chez 298 patients atteints de CCA intra-hépatique non résécable : la SG médiane était de 15,5 mois ; une réponse tumorale partielle était observée chez 28 % des patients et une stabilité chez 54 % [14]. Elle est considérée comme une option dans les CCA intra-hépatiques localement avancés et peut permettre, en association avec la chimiothérapie systémique « d’induction », d’obtenir un downstaging tumoral chez certains patients et d’envisager une résection secondaire [15]. La radiothérapie externe (par exemple, la stéréotaxie) peut aussi être proposée dans cette indication, et peut être discutée en réunion de concertation pluridisciplinaire en alternative à la chirurgie chez des patients fragiles/non opérables [16, 17]. En raison de la rareté des CVB, aucune de ces approches locorégionales n’a été évaluée dans des essais cliniques randomisés. L’étude SIRCCA (NCT02807181) évaluant la chimiothérapie par CISGEM (cisplatine et gemcitabine) seule ou associée à la radiothérapie interne sélective dans les CCA intra-hépatiques est en cours.
Traitements des formes avancées
La grande majorité des CVB (70 %-80 %) sont diagnostiqués à un stade avancé et relèvent d’un traitement par soins de support et chimiothérapie lorsqu’elle est possible [1].
Drainage biliaire
En cas de cholestase, le drainage biliaire constitue la principale mesure thérapeutique palliative en cas de tumeur non résécable ou chez les patients inopérables [1]. Il doit être réalisé avant de débuter une chimiothérapie [1].
Le caractère incomplet du drainage biliaire impacte négativement la survie et est source de morbidité (angiocholite, ictère, prurit) ; aussi le drainage doit être le plus complet possible, en privilégiant les secteurs fonctionnels et en minimisant le risque iatrogène (drainage de tout secteur opacifié, antibiothérapie) [18, 19]. En cas de tumeur complexe, il doit être confié à un centre expert possédant les compétences en endoscopie et en radiologie interventionnelle, qui doivent fréquemment être utilisées successivement ou simultanément [1].
Chimiothérapie
L’objectif de la chimiothérapie est l’augmentation de la SG, mais aussi et surtout le maintien ou l’amélioration de la qualité de vie et le contrôle des symptômes (ictère, prurit, douleur) [1].
La chimiothérapie par CISGEM (gemcitabine et cisplatine) est le standard thérapeutique dans les CVB avancés en première ligne depuis 2010 sur la base de l’essai de phase III randomisé anglais ABC-02 qui a démontré la supériorité de ce doublet par rapport à la gemcitabine seule en termes de SG (médiane : 11,7 vs. 8,1 mois, p < 0,001) et de survie sans progression (SSP) (médiane : 8,0 vs. 5,0 mois, p < 0,001) [20]. L’étude randomisée de phase II/III PRODIGE 38-AMEBICA (NCT02591030), dont les résultats sont attendus, compare la tolérance et l’efficacité du CISGEM et de l’association FOLFIRINOX modifié (5-FU, acide folinique, oxaliplatine et irinotécan) chez les patients ayant un CVB avancé.
Il n’existait pas jusqu’à récemment de standard thérapeutique de deuxième ligne [1]. L’étude ABC-06, présentée à l’ASCO en 2019, a démontré la supériorité du FOLFOX modifié (5-FU, acide folinique, oxaliplatine) par rapport aux soins de support seuls après échec d’une première ligne par CISGEM (SG médiane : 6,2 vs. 5,3 mois, HR = 0,69, p = 0,031) [21]. La chimiothérapie par CISGEM (gemcitabine et cisplatine) est le standard thérapeutique de première ligne des formes avancées
Thérapies ciblées
Les thérapies ciblées « classiques » (principalement anti-EGFR et anti-angiogéniques) ont échoué à apporter un bénéfice de survie dans le traitement des CVB dans des populations de patients non sélectionnés [22, 23]. Des études génomiques comparatives entre CCA intra-hépatiques, extra-hépatiques et adénocarcinomes de la vésicule biliaire ont permis de révéler l’hétérogénéité moléculaire de ces tumeurs et d’identifier certaines anomalies génétiques spécifiquement présentes dans certaines localisations [22, 24-28]. Ces classifications moléculaires des CVB ont ouvert la voie à des traitements bioguidés personnalisés [29].
La cohorte « CVB » de l’essai MOSCATO-01 a fourni la première preuve qu’un profil moléculaire par séquençage haut débit était faisable en pratique clinique et pouvait apporter un bénéfice chez ces patients [27]. Le taux de succès pour détecter au moins une altération moléculaire pouvant être ciblée était d’environ 70 %. L’administration de traitements ciblés sur ces anomalies a montré un bénéfice clinique (défini par le rapport SSP avec la thérapie ciblée sur SSP avec la ligne antérieure > 1,3) chez 80 % des patients et un taux de réponse objective de 33 %. Des études génomiques ont permis d’identifier certaines anomalies génétiques spécifiques de certaines localisations, ouvrant la voie à un traitement bioguidé personnalisé
Mutations IDH1
Les mutations de l’isocitrate déshydrogenase-1 (IDH1), impliquée dans le métabolisme cellulaire mitochondrial, sont présentes dans 10 % à 20 % des CCA intra-hépatiques [30]. Elles n’ont pas d’impact sur le pronostic des patients. L’ivosidénib (AG120) est un inhibiteur de la forme mutée d’IDH1. Dans une étude de phase I chez 73 patients, il avait montré un premier signal d’activité avec une SSP médiane de 3,8 mois et une SG médiane de 13,8 mois [31]. L’étude de phase III ClarIDHy, présentée à l’ESMO 2019, a montré la supériorité de l’ivosidénib, par rapport au placebo chez des patients atteints de CVB avec mutation IDH1 pré-traités (SSP : HR = 0,37, p < 0,001) [32].
Fusions FGFR2
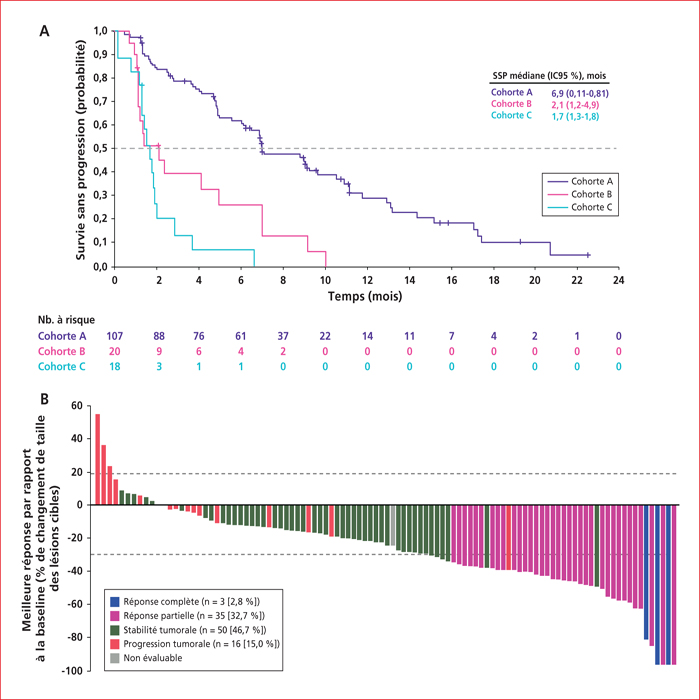
Les translocations du gène codant le récepteur 2 du fibroblast growth factor (FGFR2) sont présentes elles aussi dans 10 % à 20 % des CCA intra-hépatiques et sont associées à des survies plus favorables [30, 33]. Plusieurs molécules inhibitrices de FGFR ont été développées (tableau 1). Parmi ces molécules, le pemigatinib, inhibiteur oral de FGFR1/2/3, a fait l’objet d’une étude de phase II, FIGHT-202, dont les résultats ont été présentés à l’ESMO 2019 [34]. Cette étude a inclus des patients atteints de CCA localement avancés ou métastatiques, en progression après au moins une ligne de traitement, avec un performance status (PS) : 0-2. Les patients étaient répartis en trois cohortes : (i) tumeurs présentant une fusion ou un réarrangement de FGFR2 (cohorte A, n = 107), (ii) tumeurs avec autres altérations génétiques de FGF/FGFR (cohorte B, n = 20) et (iii) tumeurs sans altération de FGF/FGFR (cohorte C, n = 18). L’objectif principal était le taux de réponse dans la cohorte A. Les résultats sont résumés dans le tableau 2 et la figure 1. Cinquante-six fusions étaient identifiées, BICC1 étant le partenaire le plus fréquemment observé [35]. L’étude était en faveur d’une activité clinique du pemigatinib avec un taux de réponse de 35,5 %, une SSP médiane de 6,9 mois et une SG médiane de 21,1 mois. L’hyperphosphorémie était la toxicité la plus fréquente (exclusivement de grade 1-2). Une hypophosphorémie était observée chez 23 % des patients (grade 3-4 : 12 %) et un décollement séreux rétinien chez 4 % (sans séquelle). Ces toxicités étaient gérables et n’ont été à l’origine d’un arrêt du traitement que chez 9 % des patients. Une étude de phase III, FIGHT-302 (NCT03656536), est en cours évaluant le pémigatinib en première ligne vs. la chimiothérapie de référence par CISGEM chez des patients atteints de CCA avec réarrangement de FGFR2.
Cibles « agnostiques » : NTRK et MSI
Le gène NTRK code pour le récepteur TRK, un récepteur membranaire ubiquitaire dont la signalisation est associée à la voie des MAP kinases. Des fusions du gène NTRK (notamment avec ALK ou ROS1) sont observées dans3,5 % des CCA intra-hépatiques [36]. Des inhibiteurs de NTRK (entrectinib, larotrectinib) ont été développés et ont montré leur efficacité dans les tumeurs avec fusions de NTRK, ayant conduit à une ATU pan-tumeur pour le larotrectinib [37, 38].
Par ailleurs, une sous-population de CCA (< 4 %) présente un phénotype d’instabilité des microsatellites (MSI), leur conférant une sensibilité aux inhibiteurs de point de contrôle immunitaire [39]. En dehors des tumeurs MSI, les anti-PD1 (pembrolizumab, nivolumab) ont montré des taux de réponse entre 5 % et 18 % et des réponses prolongées chez certains patients [40, 41]. Plusieurs essais de phase II et III en cours évaluent des stratégies d’immunothérapie, dont l’étude française de phase II randomisée PRODIGE 57-IMMUNO-BIL (NCT03704480).
Autres cibles
D’autres altérations génétiques moins fréquentes pouvant être ciblées ont été identifiées dans les CVB et ont fait l’objet d’études spécifiques, dont une sélection est présentée dans le tableau 3.
Conclusions et perspectives
Au total, les CVB sont :
- –des tumeurs rares, de mauvais pronostic ;
- –hétérogènes sur le plan anatomique, épidémiologique et thérapeutique ;
- –dont la prise en charge est multidisciplinaire et fait appel à des centres experts (chirurgie, traitements locorégionaux, et plus récemment plateformes de génomique) ;
- –dont le traitement a évolué au cours des dernières années (standardisation de l’adjuvant et des traitements de première et deuxième ligne) ;
- –en cours de démembrement moléculaire pour les thérapies ciblées.
Les principales cibles moléculaires par localisation sont résumées dans la figure 2. L’étude SAFIR ABC 10, d’ouverture prochaine, évaluera une stratégie de maintenance guidée sur le profil moléculaire de la tumeur.
Ces évolutions récentes posent la question de la réalisation d’un profil moléculaire systématique pour ces patients, dont les modalités, en particulier le type de panel (ADN ou ARN) et le tissu cible (tumeur ou sang), et l’organisation logistique au niveau territorial restent à définir.Take home messages
Liens d’intérêts
l’auteur déclare les liens d’intérêts suivants en rapport avec l’article : Coordinatrice nationale de l’étude IMMUNOBIL PRODIGE 57 ; Co-responsable scientifique de l’étude AMEBICA PRODIGE 38 ; Interventions ponctuelles pour le laboratoire AstraZeneca (essai clinique, boards).
Cet article reprend les temps forts du symposium Incyte lors de l’ESMO 2019.
![]() This work is licensed under a
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License
This work is licensed under a
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License