Hépato-Gastro & Oncologie Digestive
MENUUlcerative jejunitis Volume 25, issue 8, Octobre 2018
Observation clinique
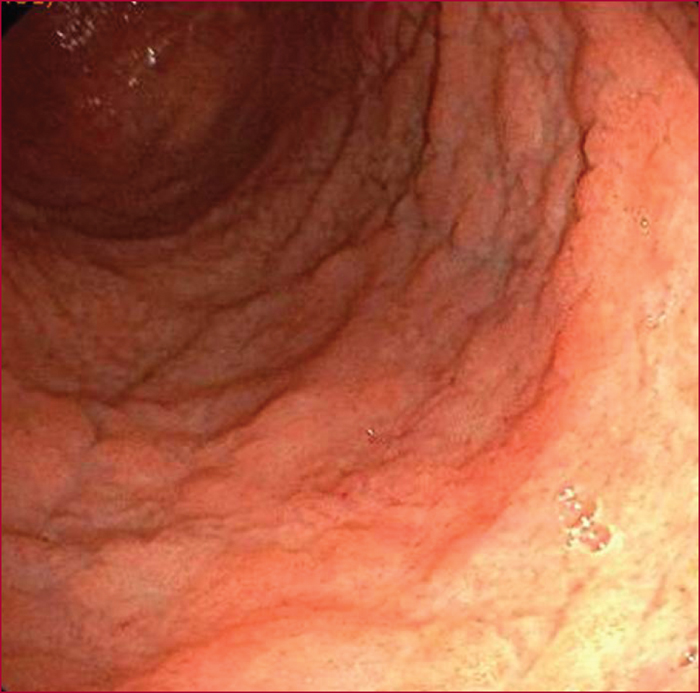
Une patiente de 42 ans, originaire d’Afrique du Nord et vivant en France depuis un an, se présente pour des diarrhées évoluant depuis un an et amaigrissement de 15 kg au cours des six derniers mois. Son principal antécédent est un kyste dermoïde de l’ovaire opéré. Sa taille est 1,65 m pour un poids de 45 kg. Le bilan biologique montre une anémie microcytaire à 9 g/dL et une hypoalbuminémie à 20 g/L. La sérologie VIH est négative. La coloscopie est macroscopiquement normale. On peut voir à la figure 1 l’aspect de la muqueuse duodénale visible au cours de l’endoscopie œsogastroduodénale.Question n̊1. Comment décrire l’aspect macroscopique ?
Question n̊2. Quels autres examens réalisez-vous ?
- a)Dosage des anticorps anti-transglutaminase
- b)Bilan martial
- c)Dosage de la vitamine B12
- d)HLA de type II
- e)Biopsies duodénales
Le dosage des anticorps anti-transglutaminases et la réalisation des biopsies duodénales (deux dans le bulbe et quatre dans le deuxième duodénum) sont nécessaires au diagnostic de maladie cœliaque suspecté sur l’aspect macroscopique d’atrophie villositaire. Le bilan complémentaire de malabsorption comporte le bilan phosphocalcique, la recherche d’une carence martiale et en folates trouvée chez environ 60 à 70 % des patients au diagnostic de maladie cœliaque et de façon moins fréquente en vitamine B12 (≈ 30 %) [1]. La détermination du typage HLA de type II n’est pas nécessaire à ce stade du diagnostic.
Poursuite de l’observation
Le dosage des anticorps IgA anti-transglutaminase est positif et l’examen anatomopathologique des biopsies duodénales décrit une atrophie villositaire totale avec augmentation des lymphocytes intraépithéliaux à 90 pour 100 cellules épithéliales. La patiente est mise au régime sans gluten. Il n’existe aucune amélioration trois mois plus tard et la patiente a perdu 3 kg supplémentaires.Question n̊3. Quels examens réalisez-vous ?
Un entéroscanner est préconisé en cas de maladie cœliaque résistante au régime sans gluten afin d’éliminer une complication maligne (lymphome, adénocarcinome du grêle) de même que le PET-scanner [2]. La vidéocapsule endoscopique peut être réalisée après élimination de sténose à l’entéroscanner pour localiser les lésions [3]. En fonction de la localisation des lésions, on pourra réaliser une entéroscopie digestive haute ou basse dans le but de les atteindre et les biopsier. La réalisation du typage HLA de type II est utile à ce stade pour éliminer une autre entéropathie avec atrophie villositaire. Un typage HLA de type II non DQ2 non DQ8 doit faire envisager un autre diagnostic comme par exemple celui d’une entéropathie auto-immune qui peut s’accompagner d’une sérologie anti-transglutaminase positive.
Poursuite de l’observation
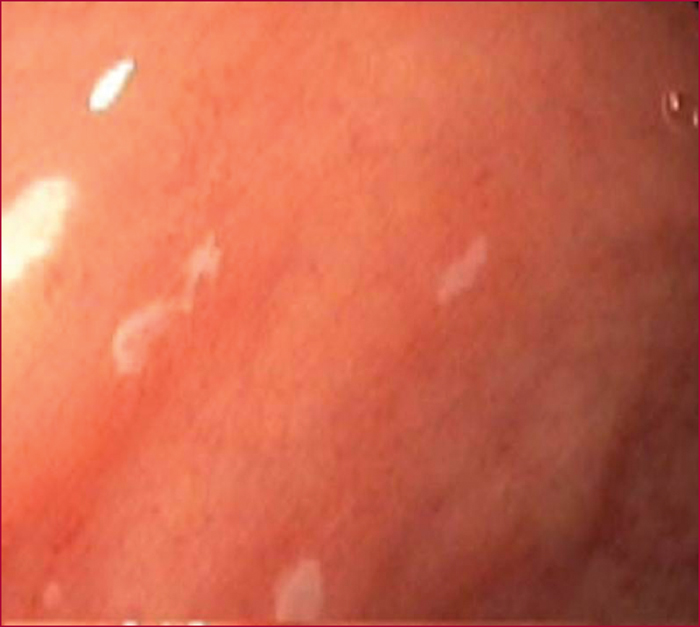
Aucune sténose du grêle n’est visible sur l’entéroscanner qui montre par ailleurs plusieurs adénopathies mésentériques de 1 cm à 3 cm. Il existe une fixation diffuse modérée de l’ensemble du grêle (SUV = 3) sans foyer d’hyperfixation au PET-Scan. La patiente est HLA-DQ2 homozygote. Il existe un aspect de jéjunite ulcéreuse en vidéocapsule incluant plusieurs ulcérations supracentimétriques biopsiées au cours de l’entéroscopie digestive haute (figure 2).Question n̊4. Quel diagnostic est le plus probable ?
Le diagnostic le plus probable est celui de SRII caractérisée par une jéjunite ulcéreuse dans 70 % des cas au diagnostic [4] et responsable d’une entéropathie exsudative comme dans le cas présent (albumine : 20 g/L) (encadré 1). Même si des ulcérations jéjunales ont été décrites au cours de la SRI, elles sont rares et infracentimétriques. Les adénopathies mésentériques supracentimétriques sont habituelles en cas de SRII [4]. L’absence de fixation significative au PET-Scanner est contre le diagnostic de lymphome invasif (enteropathy associated T cell lymphoma) qui fixe fortement contrairement à la SRII. Même si le risque de développer une maladie inflammatoire chronique de l’intestin au cours d’une maladie cœliaque est multiplié par 10, l’association avec une maladie de Crohn reste rare [5].Question n̊5. Quelles techniques sont utiles pour confirmer le diagnostic ?
La SRII est caractérisée par un trou phénotypique immunohistochimique au niveau des lymphocytes intraépithéliaux (LIE) : CD3+ (marquage intracytoplasmique), CD8- et par un réarrangement clonal du récepteur T. À l’inverse, les LIE de la SRI ont un phénotype normal en immunohistochimie CD3+CD8+ et un répertoire polyclonal [4]. Le phénotypage des LIE extraits de l’intestin confirme le phénotype anormal des LIE de la SRII avec l’absence d’expression en surface du CD3, CD8 et du récepteur T. La moitié des patients avec SRII ont une population circulante anormale au moment du diagnostic (phénotypage lymphocytes du sang veineux périphérique) [4].Question n̊6. Quels traitements sont utilisés au cours de la sprue réfractaire de type II ?
Les corticoïdes généraux sont très souvent utilisés et efficaces sur le plan clinique avec des effets histologiques partiels [4] mais sont supplantés par le budésonide plus facile en utilisation chronique du fait de la corticodépendance avec des règles spécifiques d’utilisation comme l’ouverture de la capsule de budésonide dans la bouche et le broyage par les dents [6]. Les analogues de purine telles que la cladribine, fludarabine ou pentostatine sont les drogues de chimiothérapie les plus efficaces à coupler idéalement à une autogreffe de moelle [7-9]. Les anticorps anti-IL15 n’ont été à ce jour utilisés que sous la forme d’un essai clinique en cours d’évaluation [10].Questions n̊7. Quels sont les risques évolutifs de la sprue réfractaire de type II ?
Le taux de mortalité est élevé au cours de la SRII du fait de la malnutrition, de la morbidité et de la fréquente transformation en lymphome invasif (EATL) [4]. Il n’existe pas d’association particulière décrite entre SRII et adénocarcinome du grêle dont le risque est augmenté de façon générale au cours de la maladie cœliaque. Il existe un risque de syndrome occlusif au cours de la SRII en raison de la possibilité de sténoses de grêle.Bonnes réponses aux questions
Take home messages
- •Le terme de jéjunite ulcéreuse fait référence de façon générale à des ulcérations du grêle proximal.
- •Les causes sont diverses principalement infectieuses, inflammatoires, néoplasiques, ischémiques ou médicamenteuses.
- •La forme typique de jéjunite ulcéreuse doit faire chercher une sprue cœliaque réfractaire maligne de type II, lymphome intraépithélial de bas grade caractérisé par un trou phénotypique.
- •Des études anatomopathologiques spécialisées, phénotypiques et moléculaires peuvent être nécessaires au bilan d’une jéjunite ulcéreuse pour éliminer notamment une lymphoprolifération intestinale.
Liens d’intérêts
participation à un essai clinique en tant que co-investigateur (Celimmune).
![]() This work is licensed under a
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License
This work is licensed under a
Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License