Médecine thérapeutique / Pédiatrie
MENULe suivi à long terme après traitement d’une leucémie aiguë de l’enfant : enjeux, acquis et perspectives Volume 22, numéro 2, Avril-Mai-Juin 2019
Introduction
Longtemps les pédiatres chargés du traitement des leucémies de l’enfant et de l’adolescent se préoccupaient presque exclusivement d’améliorer les chances de survie de leurs patients ou, à défaut, de les accompagner dans un parcours palliatif. Des progrès thérapeutiques considérables ont transformé la conjoncture : les guérisons sont désormais fréquentes et souvent sans aucune séquelle décelable. Cependant, la maladie elle-même, la lourdeur des thérapeutiques, les difficultés du parcours, exposent à des effets secondaires tardifs qui peuvent retentir sur l’état de santé, la qualité de vie et l’insertion sociale, longtemps après la fin des traitements [1, 2]. Un nouveau chapitre de la cancérologie pédiatrique fut ainsi ouvert et, malgré la richesse de l’expérience acquise au cours des vingt dernières années dans le domaine, bien des aspects restent à écrire. Habituellement défriché par des cancérologues pédiatres, le sujet est naturellement très ouvert sur la pédiatrie générale et les autres spécialités pédiatriques, avec l’ambition partagée de mener ces enfants jusqu’à une vie d’adulte la plus normale possible.
L’enjeu du suivi à long terme est double : prise en charge individuelle des patients et amélioration de nos connaissances. À l’échelle individuelle, le suivi prolongé a pour ambition d’améliorer l’état de santé du patient par le dépistage, la prise en charge précoce des séquelles et si possible par leur prévention. Il doit être personnalisé, c’est-à-dire adapté au risque réel de séquelles et particulièrement au type de traitement reçu. À l’échelle collective, l’amélioration de nos connaissances passe par la constitution de cohortes prospectives sur lesquelles des travaux scientifiques de qualité puissent être menés. En France, le programme LEA (pour Leucémie Enfants Adolescents) est dédié au suivi prolongé après traitement d’une leucémie de l’enfance [3]. Programme de soin autant que de recherche, il repose sur la constitution d’une cohorte prospective multicentrique composée de plus de 5 000 patients dans 17 centres français de cancérologie pédiatrique. Une part importante des données décrites dans le texte qui suit sont issues de cette cohorte.
Description de l’état de santé physique et facteurs de risques identifies
L’état de santé physique des adultes guéris de leucémies de l’enfance peut être entièrement normal. Des effets secondaires tardifs sont cependant possibles, liés à la maladie elle-même, aux traitements reçus et sans doute également à des susceptibilités individuelles (tableaux 1 et 2). Les thérapeutiques les plus pourvoyeuses de séquelles tardives sont l’irradiation cérébrale prophylactique ou curative [4] et les greffes de cellules souches hématopoïétiques, notamment lorsqu’une irradiation corporelle totale est utilisée en préparation à la greffe [5]. Le recours à l’irradiation cérébrale est heureusement devenu beaucoup plus rare dans les protocoles modernes. La greffe de cellules souches hématopoïétiques reste cependant un traitement souvent utilisé, soit en première rémission pour les formes les plus graves de leucémie, soit après échec de la chimiothérapie de première intention et rechute de la maladie. Les jeunes adultes guéris après greffe sont particulièrement vulnérables [6, 7].
Croissance staturale et taille définitive
La croissance staturale peut être anormale, notamment après irradiation du système nerveux central, crânienne ou cranio-spinale, et après greffe, avec ou sans irradiation corporelle totale. Le déficit de taille peut être dû soit à une insuffisance en hormone de croissance du fait de l’irradiation hypophysaire, soit aux effets de l’irradiation sur les cartilages de conjugaison et/ou les vertèbres. Le mécanisme des atteintes secondaires aux alkylants à forte dose utilisés en préparation aux greffes est plus mal compris.
Après greffe, la poussée de croissance péri-pubertaire doit être particulièrement surveillée car c’est souvent le moment où la vélocité de croissance est la plus altérée [8]. La taille définitive après greffe dépend de la préparation utilisée avant greffe. Dans l’expérience française, après irradiation du corps entier, la taille moyenne est à 153 cm pour les femmes et 164,5 cm pour les hommes. Après les préparations par alkylants à forte dose, la taille moyenne est à 161 cm pour les femmes et 170 cm pour les hommes. Lorsqu’une atteinte significative de la croissance staturale est détectée, une exploration de l’hormone de croissance est indiquée. Les résultats des traitements par hormone de croissance sont bons [9]. Le risque d’augmenter l’incidence des secondes maladies malignes est discuté. Un sur-risque modéré de méningiome et d’ostéosarcome en zone irradié a été décrit mais jamais confirmé [10]. Ainsi considère-t-on qu’il n’y a pas de contre-indication oncologique à l’utilisation de l’hormone de croissance dans ce contexte.
Chez les enfants traités par chimiothérapie seule, sans greffe ni irradiation cérébrale, la taille définitive n’est pratiquement pas affectée.
Obésité, syndrome métabolique
On sait de longue date que le risque de surpoids et d’obésité est augmenté chez l’adulte guéri d’une leucémie de l’enfance, mais ce risque est assez limité aux patients traités par irradiation cérébrale, particulièrement lorsqu’il s’agit de filles [11]. L’irradiation cérébrale étant actuellement rarement utilisée, cette complication devrait être moins fréquente dans l’avenir.
Plus récemment, on a constaté un sur-risque de syndrome métabolique [12, 13]. Ce syndrome métabolique associe au moins trois des cinq anomalies suivantes : obésité abdominale, hypertriglycéridémie, diminution du cholestérol HDL, augmentation de la glycémie à jeun, hypertension artérielle. Il augmente fortement le risque cardiovasculaire ultérieur.
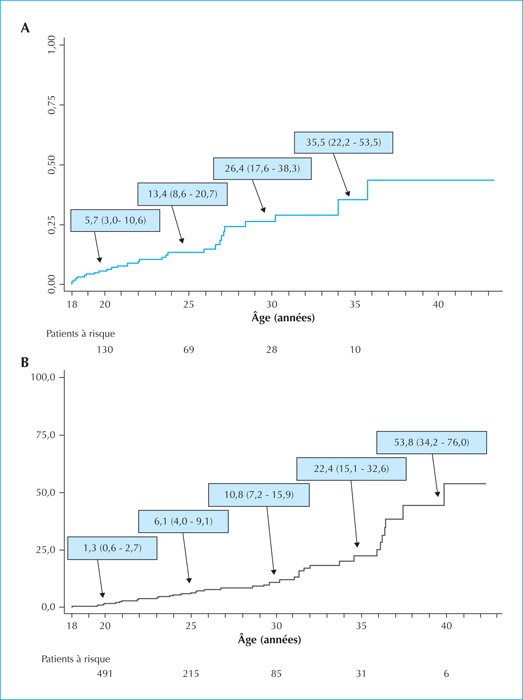
Cette complication a été particulièrement étudiée en France dans la cohorte LEA et nous avons pu tracer des courbes de survenue du syndrome métabolique au cours du temps. Comme le montre la figure 1, la probabilité de survenue ne cesse d’augmenter avec l’âge des patients [14-16]. En comparant les prévalences observées dans la cohorte LEA avec une cohorte en population générale française de grande envergure (cohorte IPC, « Investigations Préventives et Cliniques »), nous avons montré que le syndrome métabolique est plus fréquent chez les leucémiques guéris, quel que soit le traitement reçu [17] (chimiothérapie seule, chimiothérapie et irradiation cérébrale, greffe avec ou sans irradiation corporelle totale).
Il apparaît maintenant que l’aspect du syndrome métabolique et probablement sa physiopathologie dépendent du traitement reçu. C’est ainsi que les patients qui ont reçu une irradiation corporelle totale sont beaucoup moins souvent obèses que les autres, alors même que leurs perturbations métaboliques sont plus graves et plus fixées dans le temps. Des travaux physiopathologiques récents de notre groupe suggèrent que l’irradiation corporelle totale altère la fonction des cellules souches adipeuses du tissu adipeux sous-cutané. Ceci diminue la capacité de stockage des graisses dans le tissu adipeux normal et favorise ce stockage dans des sites ectopiques, notamment au niveau du foie [18]. La physiopathologie du syndrome métabolique chez les patients qui n’ont pas eu d’irradiation corporelle totale reste mal comprise. Les corticoïdes ne sont probablement pas en cause. Il est possible mais non prouvé que les alkylants à forte dose aient un effet « irradiation-like » sur les cellules souches adipeuses.
Fonction gonadique et fertilité
Les adultes guéris d’une leucémie aiguë après un protocole de chimiothérapie de première ligne habituel ont une fonction gonadique et une fertilité normale. Leurs enfants n’ont pas de risque particulier de maladie maligne ni de malformation congénitale [19]. Pour ceux qui ont reçu des chimiothérapies particulièrement lourdes, avec notamment des doses conséquentes d’agents alkylants, le risque est intermédiaire avec un risque de ménopause précoce chez la femme.
Malheureusement, la situation est très différente pour les patients guéris après une greffe de cellules souches hématopoïétiques. Les données LEA permettent de distinguer plusieurs situations. Après irradiation du corps entier chez le garçon, la production de testostérone est normale dans la moitié des cas (avec souvent cependant une augmentation des taux sériques de LH) mais l’azoospermie est presqu’inéluctable. Chez la femme irradiée après la puberté, une insuffisance gonadique hypergonadotrope définitive est quasi-constante mais ceci n’est pas vrai lorsque l’irradiation corporelle totale a été effectuée chez la fille très jeune. Dans ces cas, des pubertés spontanées normales peuvent survenir et des grossesses sont alors parfois possibles, avec cependant des difficultés supplémentaires liées à l’irradiation utérine. Ces atteintes radiques de l’utérus peuvent entraîner des avortements spontanés à répétition, un risque plus élevé de prématurité, de petit poids de naissance et de complications pendant l’accouchement. Les mêmes difficultés sont attendues lorsque la grossesse est obtenue après don d’ovocytes.
Les garçons qui ont eu du busulfan en préparation de la greffe ont une production de testostérone normale dans trois quarts des cas mais leur LH est souvent augmentée et leur fertilité, bien qu’encore mal évaluée, est probablement très diminuée. Chez la fille traitée par busulfan avant l’âge pubertaire, l’insuffisance gonadique hypergonadotrope est quasiment systématique, sauf peut-être lorsque le traitement a été donné chez une très jeune fillette.
L’indication et les méthodes de préservation de la fertilité dépendent fortement du contexte. Chez la fille, quel que soit son âge, la préservation de la fertilité n’est pas indiquée au moment de la première poussée de la maladie si une chimiothérapie simple (sans greffe de cellules souches hématopoïétiques) est prévue, car elle retarderait le traitement à visée anti-leucémique. Lorsqu’il y a un risque de ménopause précoce, on pourra proposer après la fin du traitement un prélèvement d’ovocytes généralement au début de l’âge adulte. Si une greffe est prévue, on peut proposer un prélèvement de cortex ovarien pour cryoconservation. Après réimplantation, des grossesses ont été obtenues en dehors du contexte de leucémie. Néanmoins, le risque potentiel de réintroduction de cellules malignes est à prendre en compte, problème que des progrès futurs de folliculogenèse in vitro pourraient permettre de contourner.
Chez le garçon pubère, le prélèvement de sperme est systématiquement proposé et généralement bien accepté même chez le jeune adolescent. Chez le garçon pré-pubère pour qui une greffe est envisagée, un prélèvement de tissu testiculaire par biopsie pour cryoconservation peut être effectué. La réutilisation de ce tissu ou de cellules germinales reste du domaine de la recherche. Dans l’espèce humaine, la maturation in vitro des cellules germinales, qui permettrait d’obtenir des spermatozoïdes en vue de fécondation in vitro (pour éviter le risque de réintroduction de cellules leucémique par autogreffe de ce tissu), n’est actuellement pas encore possible.
Fonction thyroïdienne
Après irradiation de la thyroïde, une insuffisance thyroïdienne est fréquente [20, 21]. Le bilan hormonal doit être surveillé annuellement de manière prolongée car l’insuffisance apparaît après un délai de plusieurs années. Au début, l’insuffisance thyroïdienne est compensée par une élévation de la TSH. Certaines hypothyroïdies compensées sont transitoires et il ne faut pas se précipiter sur un traitement hormonal substitutif. Les alkylants à forte dose peuvent également entraîner une hypothyroïdie mais ceci est assez rare.
Cœur et vaisseaux
Le principal facteur de risque d’une atteinte de la fonction myocardique est la dose cumulée d’anthracycline. Le sexe féminin, le jeune âge au moment du traitement et l’irradiation cardiaque sont des facteurs favorisants. Une surveillance prolongée par échographie cardiaque est nécessaire car la survenue de l’insuffisance myocardique est souvent très tardive. Probablement du fait de l’attention particulière portée aux doses cumulées d’anthracycline dans les protocoles de ces trois dernières décennies, cette complication est finalement peu fréquente chez les patients guéris par chimiothérapie après une seule poussée de la maladie, même dans les leucémies aiguës myéloblastiques qui nécessitent les plus fortes doses [22]. La fréquence augmente nettement chez les patients guéris après rechute de leur maladie, car les doses d’anthracycline sont alors plus élevées du fait des deux séquences thérapeutiques. Ces situations pourraient justifier l’utilisation de cardioprotecteurs malgré l’absence de consensus en France sur le sujet.
L’irradiation des coronaires ou des vaisseaux cérébraux, ainsi que la survenue d’un syndrome métabolique, sont susceptibles d’augmenter le risque de coronaropathie et d’accident vasculaire cérébral.
Œil
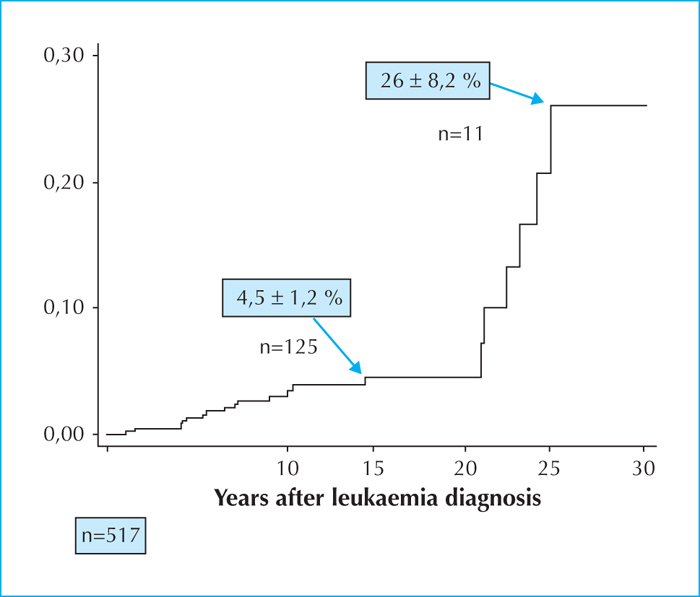
L’irradiation du corps entier donne des cataractes fréquentes (figure 2), en général peu évolutives [23]. Cette complication est également possible après irradiation cérébrale isolée, car la dose diffusée reçue par le cristallin n’est pas nulle. On a pu craindre que la corticothérapie prolongée puisse également générer cette complication chez des enfants non irradiés. L’expérience LEA est relativement rassurante car, dans la fourchette de dose cumulée de corticoïde utilisée, le risque de cataracte est très faible à quinze ans pour les patients traités sans irradiation cérébrale [24]. Cependant, un suivi plus prolongé est nécessaire avant de conclure, du fait de la survenue très tardive de cette complication.
Os et articulations
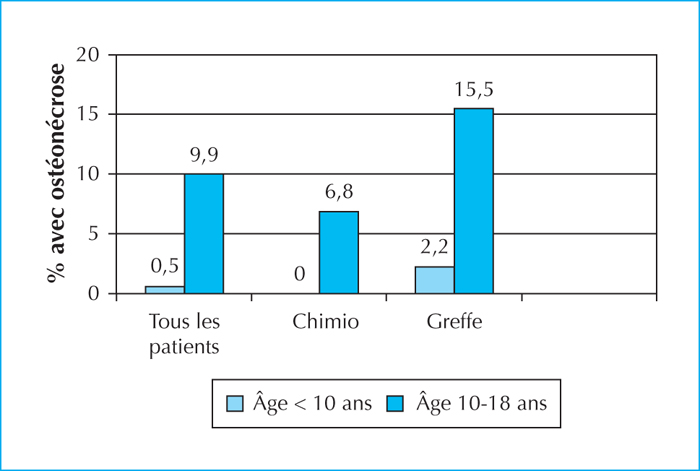
La corticothérapie peut induire des ostéonécroses, en particulier au niveau de la hanche mais également aux niveaux des genoux ou des épaules. Du fait des douleurs chroniques et de l’invalidité qu’elle engendre, cette complication a un fort impact sur la qualité de vie. Dans l’expérience LEA, l’incidence cumulée d’ostéonécrose est de 1,4 % après chimiothérapie seule et de 6,8 % après greffe de cellules souches hématopoïétiques [25]. Trois facteurs de risque ont été identifiés : une dose cumulée de stéroïdes plus élevée, un âge supérieur à dix ans au moment du diagnostic et le fait d’avoir reçu une greffe (figure 3). Enfin, on notait une atteinte très significative des domaines physiques de la qualité de vie pour les patients atteints d’ostéonécrose, par rapport à ceux qui n’avaient pas cette complication.
Il existe un risque accru d’ostéopénie et d’ostéoporose après une corticothérapie prolongée, certaines chimiothérapies et en cas d’insuffisance gonadique. La densité minérale osseuse a cependant tendance à s’améliorer à distance des traitements et à l’âge adulte, les anomalies de l’ostéodensitométries sont assez rares, sauf en cas d’insuffisance gonadique non compensée et d’invalidité prolongée liée à une ostéonécrose [26].
Tumeurs et leucémies secondaires
Le risque est faible pour les patients traités dans les protocoles de chimiothérapie moderne, sans irradiation cérébrale [27]. Les facteurs de risque sont en effet l’irradiation, les doses reçues d’inhibiteurs de topo-isomérase, d’alkylants. La susceptibilité génétique joue un rôle certain, par exemple dans les cas de maladie de Li-Fraumeni. Les principales tumeurs radio-induites sont des carcinomes thyroïdiens qui doivent être dépistés par échographie en cas d’irradiation préalable, des tumeurs cérébrales (particulièrement des méningiomes), des sarcomes, des tumeurs cutanées (carcinomes basocellulaires le plus souvent mais aussi carcinomes spinocellulaires et mélanomes) et des cancers du sein, mais de nombreuses autres tumeurs peuvent être observées. Le risque de cancer du sein après irradiation thoracique justifie sans doute un dépistage par imagerie systématique, selon des modalités proches de celles qui sont décrites dans les susceptibilités génétiques [28]. Dans la cohorte LEA, le risque après irradiation du corps entier paraît étrangement faible, peut-être seulement du fait du jeune âge des femmes adultes de la cohorte, mais peut-être aussi du fait de l’atteinte gonadique associée.
Autres complications
Le busulfan entraîne souvent une alopécie partielle définitive. Les traitements par aminosides et vancomycine peuvent être responsables d’hypoacousie.
Qualité de vie, scolarité et insertion professionnelle
La survenue d’effets secondaires tardifs est susceptible d’altérer la qualité de vie et le devenir social des patients mais les relations entre séquelles et qualité de vie sont complexes. Une première étude LEA comparait la qualité de vie des patients selon qu’ils avaient reçu ou non une greffe de cellules souches hématopoïétiques [6]. Les patients greffés avaient clairement plus de séquelles physiques que les autres. Pourtant, leur qualité de vie était strictement identique dans ses domaines psycho-sociaux. Dans les domaines physiques, on constatait quelques différences statistiquement significatives mais de très faible amplitude. Des phénomènes de compensation semblent survenir pour améliorer le vécu de handicaps modérés. Une seconde étude sur le sujet, menée sur un nombre de patients très supérieur confirmait ce paradoxe [7] et rajoutait une comparaison avec les données de qualité de vie en population générale française, ajustée selon le sexe et l’âge. Que les patients aient reçu ou non une greffe de cellules souches hématopoïétiques, les paramètres psycho-sociaux de la qualité de vie des adultes guéris d’une leucémie aiguë traitée durant l’enfance étaient significativement inférieurs à la population générale. Il est possible que, par-delà les traitements réalisés et au-delà des séquelles physiques, la qualité de vie des patients puisse être directement influencée par la maladie elle-même et son vécu.
La scolarisation et l’insertion professionnelle sont deux autres aspects fondamentaux [29, 30]. Les études effectuées aux États-Unis montrent que l’insertion professionnelle des adultes guéris d’un cancer de l’enfance est moins bonne que celle de la population générale. Cela n’est pas tout à fait le cas dans notre pays, peut-être du fait d’un système social différent. Nos résultats montrent ainsi que le taux de chômage est plutôt plus faible chez les leucémiques guéris qu’en population générale, mais que les anciens patients acceptent plus souvent des emplois précaires avec des contrats à durée déterminée.
Quelques perspectives
Identifier des susceptibilités génétiques aux effets secondaires tardifs
Si la responsabilité des traitements sur les effets secondaires tardifs est relativement bien comprise, une grande variabilité individuelle est observée à exposition thérapeutique identique, ce qui suggère une susceptibilité génétique sous-jacente. L’identification de ces susceptibilités génétiques pourrait dans l’avenir avoir des conséquences importantes sur la prise en charge des patients, en adaptant mieux les programmes thérapeutiques ainsi que la prévention, détection et prise en charge précoces des complications de l’après-cancer (action 8.2 du Plan cancer national en cours). Bien qu’il s’agisse d’une approche récente, les connaissances dans ce domaine augmentent rapidement, notamment pour les toxicités cardiaques, l’ostéonécrose, l’encéphalopathie liée au méthotrexate et les secondes tumeurs [31-39]. Le programme Gen-LEA actuellement en cours a pour objectif d’identifier des facteurs génétiques associés à la survenue de quatre effets secondaires particulièrement graves, mettant en jeu la vie des patients ou susceptible d’altérer fortement leur qualité de vie : le syndrome métabolique, la cardiomyopathie aux anthracyclines, les seconds cancers et l’ostéonécrose symptomatique.
Évaluer périodiquement les algorithmes d’exploration
Le programme de suivi doit être évolutif dans ses algorithmes d’exploration. L’expérience de LEA et d’autres cohortes de suivi à long terme permet de définir des profils de patients à risque de séquelle différent. La nature et le rythme des évaluations peuvent sans doute être diminués pour les patients à faible risque de séquelle. Dans le même temps, d’autres besoins apparaissent, qu’il s’agisse de l’application de consensus nouveaux (par exemple, le dépistage des cancers du sein après irradiation thoracique ou dépistage des méningiomes après irradiation cérébrale) ou d’explorations nouvelles dans un cadre de recherche clinique (par exemple, l’étude fonctionnelle de l’utérus irradié) ou, enfin, du suivi à long terme de nouveaux traitement dont on ignore encore largement les conséquences à long terme.
Optimiser le parcours des patients sur le long terme
La prise en charge des enfants atteints de leucémie nécessite des interactions fortes et le partage des connaissances acquises en hémato-cancérologie pédiatrique avec le pédiatre généraliste et avec les pédiatres des autres surspécialités. À l’âge adulte, le même modèle d’interaction doit être favorisé avec les médecins généralistes et spécialistes d’adulte. Dans l’avenir, la mise en place d’unités de suivi à long terme après cancer de l’enfant, de l’adolescent et de l’adulte jeune pourrait être extrêmement utile en permettant à la fois la coordination d’un suivi décentralisé et multidisciplinaire et la centralisation des connaissances.Points à retenir
Remerciements
L’étude LEA est financée par le programme hospitalier de recherche clinique, l’INCa, l’association Laurette Fugain, la ligue contre le cancer, le laboratoire MSD, l’ANR, le cancéropôle PACA, l’IRESP, la fondation BMS, l’agence de biomédecine. CONECT-AML (COllaborative Network for Children and Teenagers with Acute Myeloid Leukemia) est financé par une subvention de l’Institut National du Cancer, la Ligue contre le cancer et la fondation ARC (InCa-ARC-LIGUE_11905).
Liens d’intérêts
les auteurs déclarent n’avoir aucun lien d’intérêt en rapport avec l’article.
![]() Cette œuvre est mise à disposition selon les termes de la
Licence Creative Commons Attribution - Pas d'Utilisation Commerciale - Pas de Modification 4.0 International
Cette œuvre est mise à disposition selon les termes de la
Licence Creative Commons Attribution - Pas d'Utilisation Commerciale - Pas de Modification 4.0 International