Hématologie
MENULes anti-BCMA dans la prise en charge du myélome multiple réfractaire Volume 29, numéro 2, Mars-Avril 2023
- DOI : 10.1684/hma.2023.1811
- Page(s) : 107-20
- Année de parution : 2023
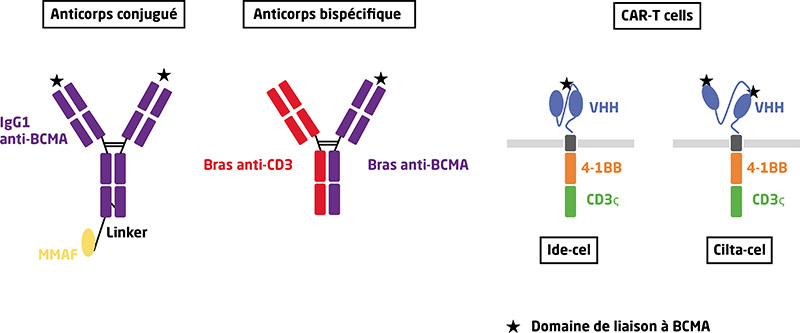
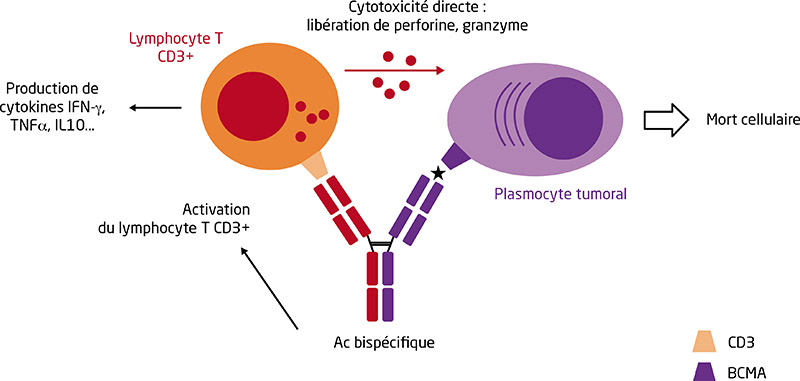
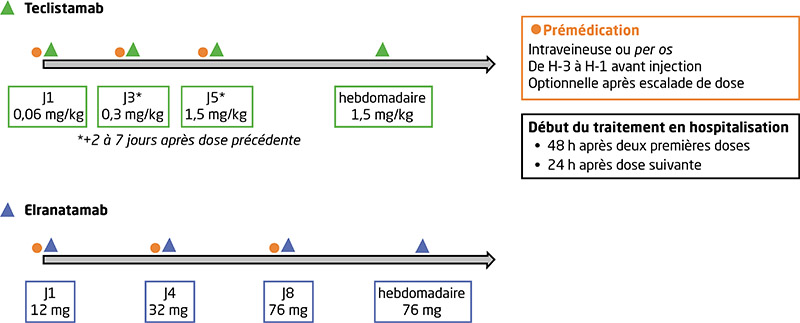
De nombreuses molécules anti-BCMA (pour B-cell maturation antigen) ont été développées ces dernières années, ouvrant de nouvelles perspectives thérapeutiques pour la prise en charge des patients atteints de myélome multiple réfractaire, en particulier chez ceux exposés ou réfractaires aux inhibiteurs du protéasome, aux immunomodulateurs et aux anti-CD38. L’idécabtagène vicleucel (ide-cel) et le ciltacabtagène autoleucel (cilta-cel) sont deux traitements par cellules T à récepteur antigénique chimérique (CAR-T cells) anti-BCMA. Les essais KarMMa et CARTITUDE ont permis de démontrer l’efficacité de ces traitements dans une population de patients triple réfractaires. Les taux de réponse globale (RG) sont de plus de 70 %, avec une proportion non négligeable de patients atteignant une maladie résiduelle négative < 10-5. Les médianes de survie sans progression (SSP) sont également significativement supérieures aux traitements de rattrapage standard. Les taux de réponses et la SSP semblent encore meilleurs avec le cilta-cel qu’avec l’ide-cel, mais son accès est plus limité. Les complications principales de ce traitement sont le syndrome de relargage cytokinique (SRC), fréquent (environ 80 % des patients) mais majoritairement peu sévère, et la neurotoxicité spécifique, qui survient chez environ 20 % des patients. Les données des essais cliniques semblent se confirmer dans une étude de vie réelle conduite aux États-Unis. Le téclistamab et l’elranatamab sont deux anticorps bispécifiques disponibles en accès précoce en France actuellement. Là aussi, les résultats des essais cliniques MajesTEC et MagnetisMM sont très prometteurs, avec des taux de RG d’environ 60 %, et une durée de SSP d’un peu moins de un an, chez des patients réfractaires et lourdement traités auparavant. Les effets secondaires principaux sont la toxicité hématologique (neutropénie surtout), majoritairement de grade 3-4, et les infections, qui concernent environ 60 % des patients. Les SRC sont fréquemment rapportés, et majoritairement peu sévères ; la neurotoxicité n’est rapportée que de manière marginale. Les combinaisons avec d’autres molécules, ainsi que l’utilisation de ces traitements à des phases plus précoces, sont des perspectives intéressantes, qui changeront peut-être nos pratiques dans les années à venir. La disponibilité limitée des CAR-T cells reste toutefois aujourd’hui un frein majeur à une prescription plus large.