Hématologie
MENURôle des rétroéléments dans l’hématopoïèse lors du vieillissement des cellules souches hématopoïétiques et dans les leucémies : ami ou ennemi ? Volume 29, numéro 1, Janvier-Février 2023
- DOI : 10.1684/hma2023.1777
- Page(s) : 30-46
- Année de parution : 2023
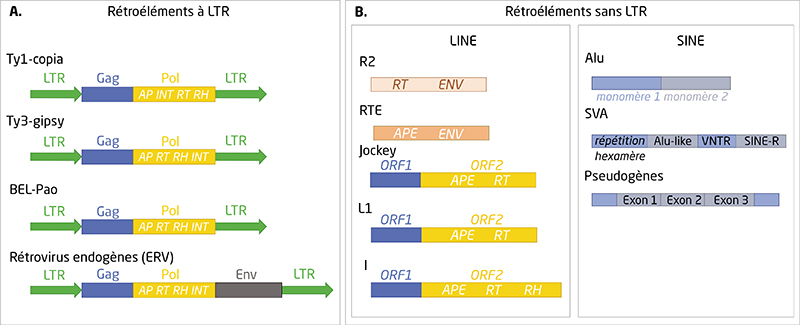
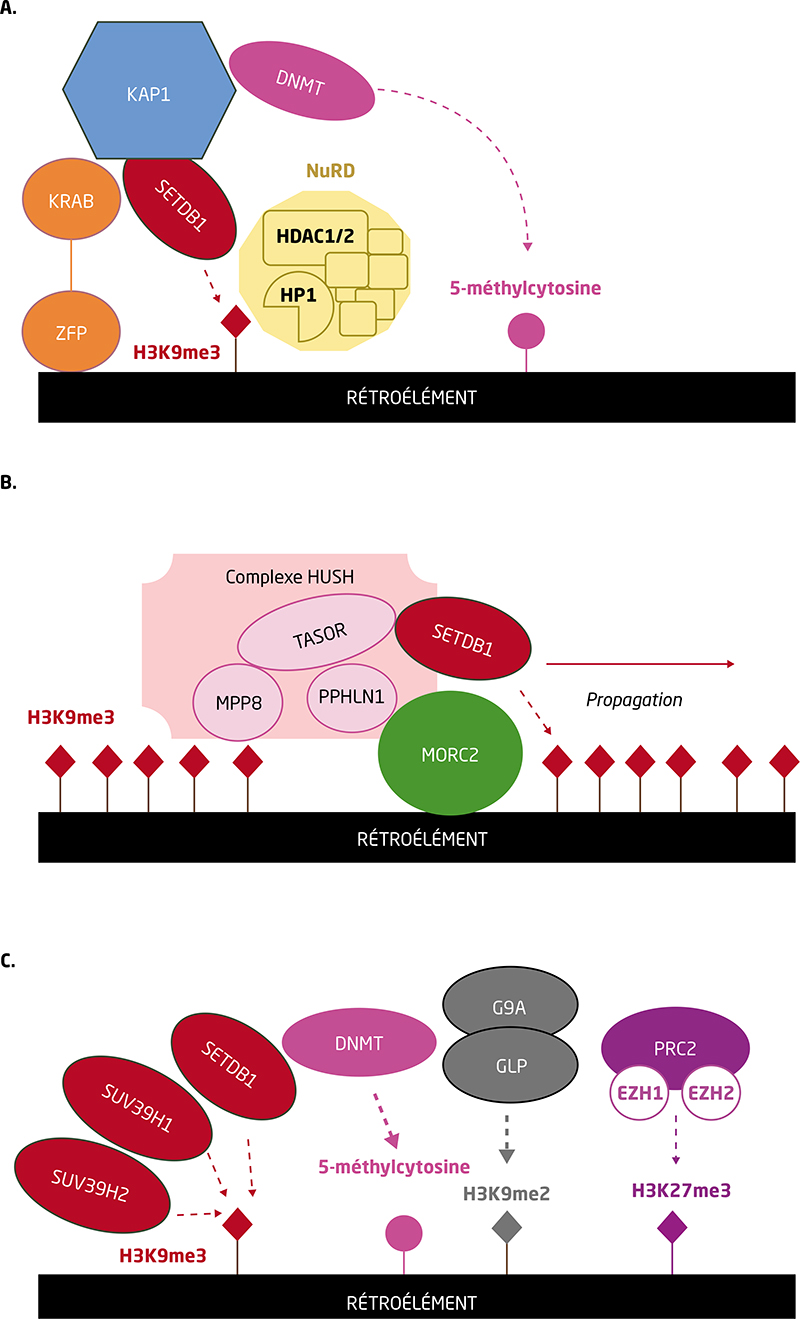
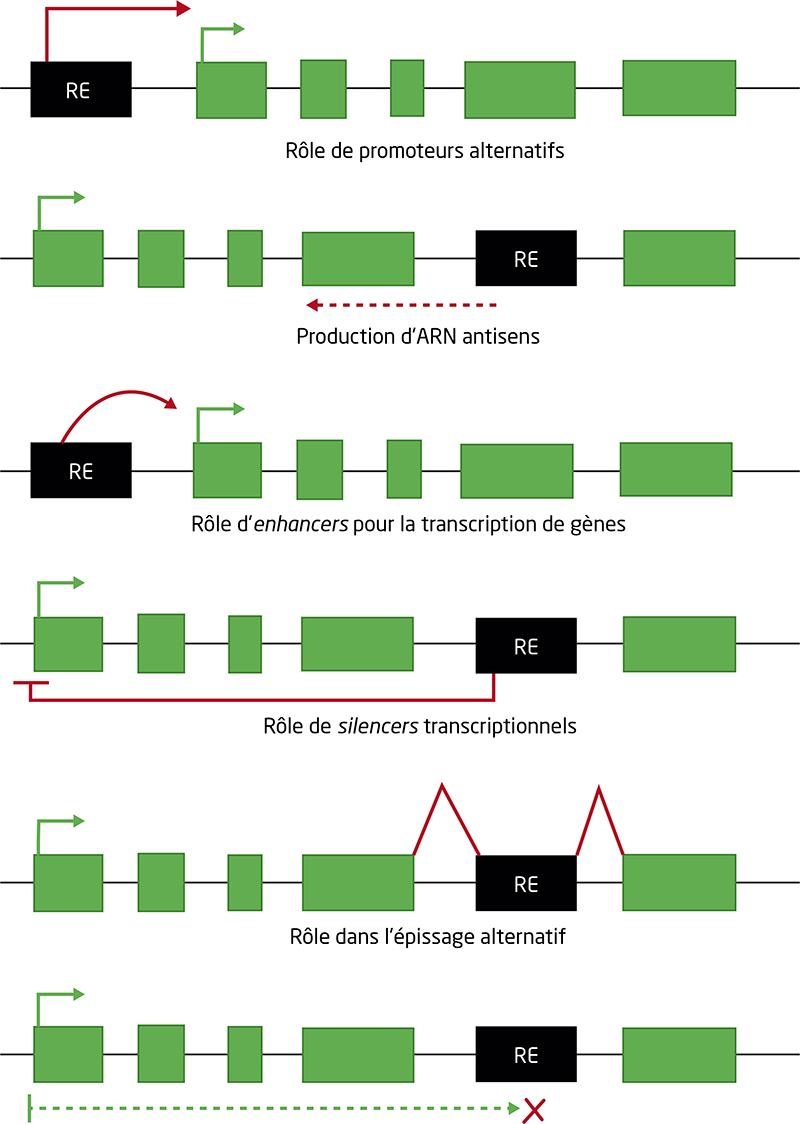
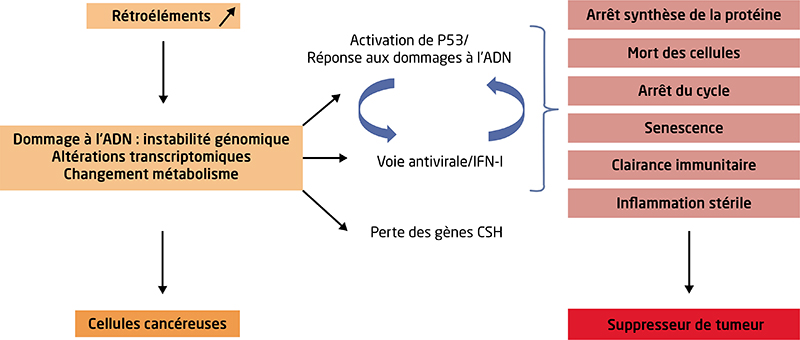
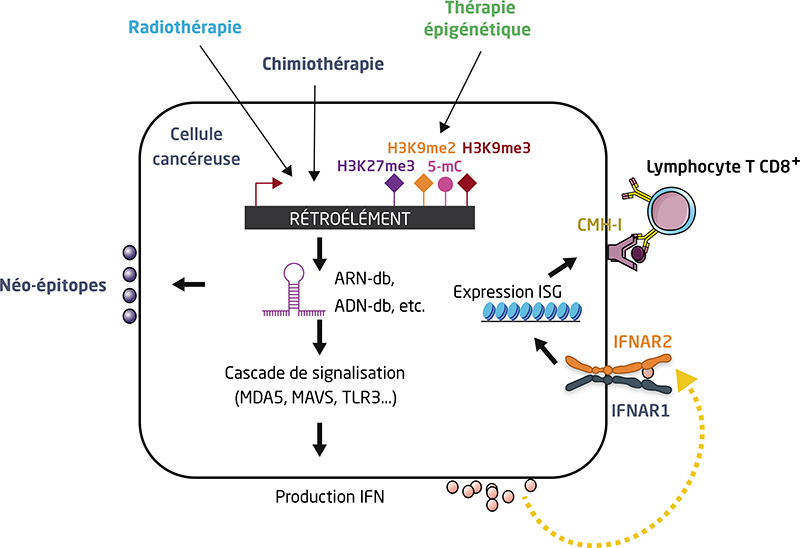
Les rétroéléments (RE), parmi lesquels les rétrovirus endogènes (ERV) et les éléments intercalés longs ou courts (LINE-1 et SINE), représentent près de la moitié des génomes humains. Les ER sont régulés par l’hétérochromatine, un état condensé de l’ADN caractérisé par la méthylation de l’ADN et des marques d’histones répressives telles que H3K9me2, H3K9me3 et H3K27me3. Longtemps décrits comme de l’ADN poubelle, ils suscitent de plus en plus d’intérêt, notamment dans le vieillissement et le cancer où la chromatine est désorganisée. Les RE peuvent se propager dans le génome par un mécanisme de copier/coller, constituant une grande source d’instabilité génomique. Ils sont également des contributeurs majeurs des réseaux de régulation des gènes, en fournissant des promoteurs alternatifs, des signaux d’épissage ou de polyadénylation, ainsi qu’en servant d’éléments cis-régulateurs, de manière spécifique, aux cellules et aux tissus. Elle est liée à la perte progressive de l’hétérochromatine. Des défauts dans la répression des RE sont également observés dans le cancer. Les cellules cancéreuses deviennent dépendantes des RE en raison de leur capacité à induire une instabilité génomique et à déréguler le transcriptome. La réactivation épigénétique de séquences régulatrices cryptiques au sein des RE existants conduit à une expression généralisée des oncogènes. Cependant, les RE sont des épées à double tranchant pour le cancer. En effet, de par leur capacité à imiter un état viral, conduisant à l’activation de l’interféron de type I, les RE peuvent déclencher une signalisation apoptotique et antiproliférative. Les thérapies anticancéreuses telles que la chimiothérapie, la radiothérapie, l’immunothérapie et les agents hypométhylants de l’ADN (HMA) utilisent cette vulnérabilité pour tuer les cellules cancéreuses. L’expression de RE étant susceptible d’être leur talon d’Achille, les cellules tumorales développent des mécanismes pour empêcher la libération de RE de la répression épigénétique. Les cellules souches leucémiques de la leucémie myéloïde aiguë ont une faible expression de RE et inactivent les voies immunitaires, ce qui peut être impliqué dans leur évasion immunitaire. Des acteurs épigénétiques tels que MPP8 et SETDB1 (pour SET domain bifurcated 1) ont été identifiés comme jouant un rôle majeur dans la répression des RE et leur dysfonctionnement est associé à la leucémogenèse. L’échec des traitements par HMA à éliminer les clones mutés observés dans les syndromes myélodysplasiques pourrait être dû à l’absence d’induction de RE. Nous discutons ici des différents mécanismes qui pourraient empêcher l’expression des ER dans les cellules souches leucémiques, de l’importance de ces éléments dans la fonction cellulaire, l’oncogenèse et l’immunité, en soulignant l’influence des mécanismes épigénétiques dans la régulation de l’expression des ER et en examinant de quelle façon ils peuvent être exploités dans un contexte thérapeutique.