e-VEGF-IMMUNO-actu
MENULes anti-angiogéniques bientôt en traitement adjuvant ? Volume 12, numéro 1, Mars 2017
Introduction
Si les médicaments anti-angiogéniques ont montré une efficacité remarquable pour le traitement des cancers avancés et/ou métastatiques, ils sont jusqu’à présent sans effet sur la survie des patients en situation adjuvante ; pourtant les essais cliniques n’ont pas fait défaut dans les cancers pour lesquels on pouvait s’attendre à des effets importants, les cancers du côlon au premier chef. L’hypothèse principale avancée pour expliquer ces échecs est le fait que les métastases infra-cliniques sont encore trop petites pour avoir besoin d’une néo-vascularisation, ou encore qu’elles subsistent dans des niches hypoxiques de la moelle osseuse sans avoir besoin d’un apport nutritif et oxygéné important. D’autres hypothèses ont été émises : pour ce qui concerne les inhibiteurs de tyrosine kinase (ITK) à visée anti-VEGFR2, leur activité collatérale anti-PDGFR peut entraîner expérimentalement une destruction des péricytes et de l’intégrité vasculaire favorable à la dissémination métastatique, malgré un effet antitumoral potentiel [1].
Pour ne citer qu’un essai de phase III important, l’essai AVANT [2], les courbes de survie des patients atteints de cancer du côlon et traités avec et sans bévacizumab ajouté au protocole FOLFOX standard se croisent en cours de route et démontrent plutôt un effet délétère de l’adjonction de l’anti-angiogénique. De façon générale, si l’effet anti-angiogénique apparaît initialement bénéfique, il s’épuise rapidement [3, 4, 5]. Rien n’indique, à l’heure actuelle, que l’on puisse envisager à court terme l’utilisation d’anti-angiogéniques en situation adjuvante, au moins dans les localisations testées, côlon, sein et rein.
Le groupe de Kerbel à Toronto s’est posé la question de savoir si le système angiopoïétine–TIE2 n’était pas une cible préférable pour juguler l’angiogenèse des micrométastases que le système VEGF–VEGFR2. Le système angiopoïétine–TIE2 n’a jamais été associé expérimentalement à la dissémination métastatique ni à une altération de l’intégrité vasculaire, mais on sait qu’il intervient au stade précoce de la colonisation des tumeurs par les vaisseaux de l’hôte. Les auteurs ont donc exploré in vivo les effets de l’association d’un inhibiteur de l’angiopoïétine ANG2 (le CVX-060, qui est une protéine de fusion entre un anticorps et un fragment du récepteur TIE2) avec un inhibiteur du VEGFR2, le sunitinib ou le régorafénib, dans 5 modèles différents de tumeurs expérimentales afin de s’assurer de la généralité de leurs observations. Ils ont également étudié les effets d’un inhibiteur mixte de VEGFA et de ANG2, le CVX-241, protéine de fusion entre un anticorps et les fragments des récepteurs TIE2 et VEGFR2.
Double inhibition des voies VEGF et ANG dans des modèles de cancer du sein
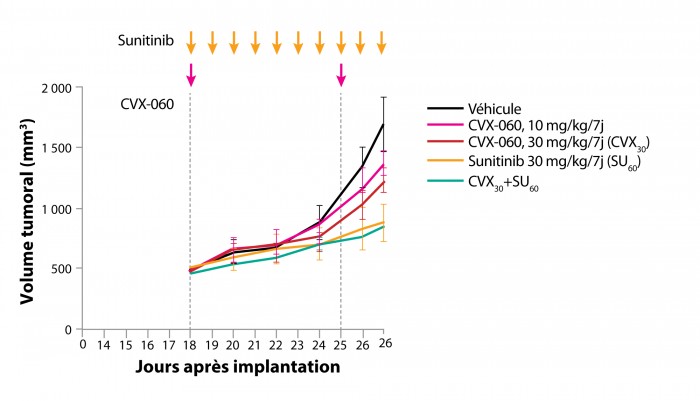
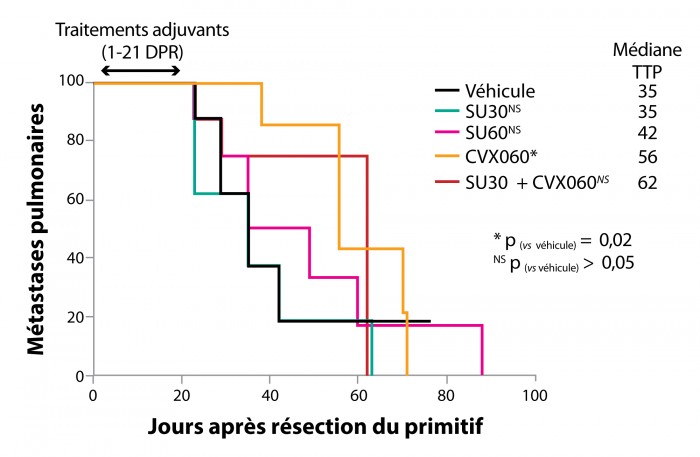
Dans un modèle orthotopique de tumeurs du sein hautement métastatiques, dérivées de la lignée MDA-MB-231 et transplantées chez des souris immunodéficientes, le CVX-060 apparaît moins actif que le sunitinib pour inhiber la croissance tumorale et son addition au sunitinib n’ajoute pas d’effet supplémentaire (figure 1). En revanche, lorsque la tumeur est retirée chirurgicalement 21 jours après implantation, le sunitinib post-chirurgical est sans effet sur la dissémination métastatique (la médiane du temps jusqu’à progression [TTP] est de 35 jours, identique à celle observée chez les souris non traitées) alors que le CVX-060 est efficace dans cette situation adjuvante, avec un TTP médian de 56 jours (figure 2) ; la combinaison des deux agents en revanche, si elle apparaît initialement efficace, n’apporte pas d’avantage par rapport au CVX-060 seul (TTP médian de 62 jours). Il est important de noter que cet effet positif du CVX-060 sur la dissémination métastatique ne se traduit pas par un effet positif sur la survie des souris.
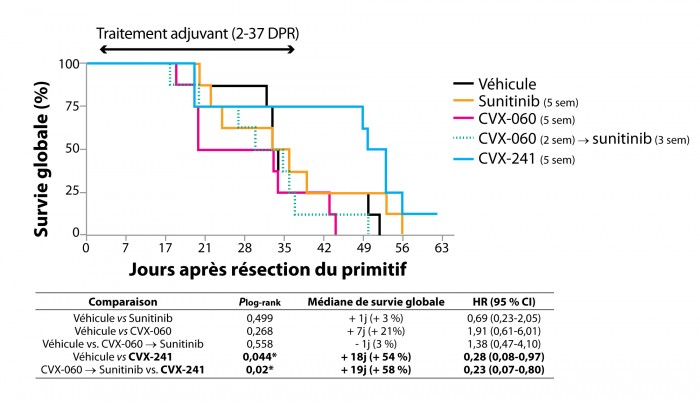
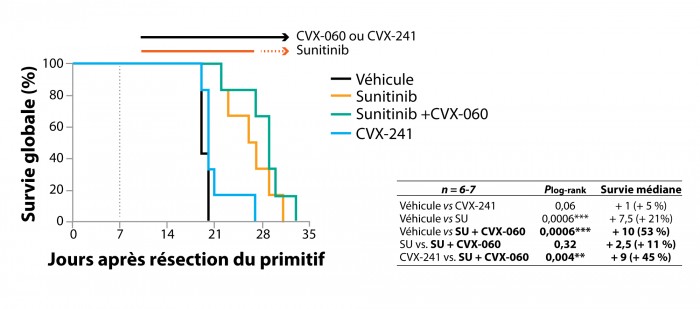
Si le CVX-060 n’apporte en définitive que très peu de résultats positifs, le CVX-241 en revanche, qui cible simultanément les deux facteurs solubles VEGFA et ANG2, apparaît efficace sur la survie des souris en administration post-opératoire (figure 3), avec un bénéfice en survie médiane de 18 à 19 jours par rapport à l’absence de traitement ou à un traitement par sunitinib et/ou CVX-060 ; des résultats comparables sont obtenus avec un autre modèle de cancer du sein opéré, syngénique et non plus xénogreffé, dérivé de la lignée murine EMT-6. À noter que dans ce modèle, un anticorps anti-PDL1 est sans effet, seul ou associé au CVX-060.
Double inhibition des voies VEGF et ANG dans des modèles de cancer du côlon
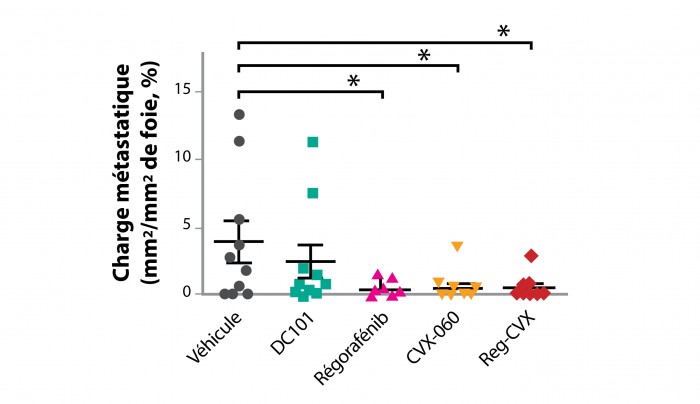
Les modèles de cancer du côlon sont deux lignées humaines relativement classiques, implantées de façon orthotopique, la lignée HCT-116, qui présente le caractère d’instabilité microsatellitaire (MSI) et possède un gène TP53 sauvage, et la lignée HT-29 qui est non-MSI et présente un gène TP53 muté. Le régorafénib est utilisé comme ITK dirigé contre VEGFR2, en notant qu’il inhibe également la kinase TIE2, alors que le sunitinib, ITK très « multicible » pourtant, n’a pas d’action sur cette kinase. Au niveau de la tumeur primaire, la croissance tumorale est inhibée de façon significative par le régorafénib dans le modèle HCT-116 mais pas dans le modèle HT-29, alors que le CVX-060 est sans effet. Pour l’étude de l’activité des molécules en situation adjuvante, les cellules tumorales sont implantées dans la rate qui est ensuite enlevée (la chirurgie est délicate et il serait difficile de priver les souris d’une partie de leur côlon…) ; au niveau hépatique, la quantification des nodules métastatiques fait apparaître un effet majeur du régorafénib (alors qu’un anticorps anti-VEGFR2, DC-101, est pratiquement sans effet), et un effet plus faible du CVX-060 et de l’association régorafénib–CVX-60 (figure 4).
Il apparaît donc que, dans ce modèle, l’ITK « bispécifique » est supérieur aux thérapies « monospécifiques » que sont l’anticorps DC-101 et la protéine de fusion CVX-060. On aurait aimé quand même voir les effets dans ce modèle de l’association DC-101–CVX-060 ou de la protéine de fusion bispécifique CVX-241. Il est toujours difficile de savoir si les expérimentations « manquantes » le sont parce que les auteurs les ont considérées comme redondantes ou parce qu’elles n’ont pas donné les résultats espérés (ou parce que les auteurs avaient épuisé leurs crédits de recherche, le cas n’est pas exceptionnel !)
Double inhibition des voies VEGF et ANG dans un modèle de cancer du rein
Troisième modèle utilisé, celui de cancers murins du rein développant spontanément des métastases pulmonaires après implantation orthotopique de cellules tumorales de la lignée RENCA. Les traitements proposés après ablation de la tumeur transplantée comportent sunitinib, CVX-060, combinaison sunitinib–CVX-060 et CVX-241 (figure 5). Résultats intéressants mais d’interprétation complexe. Dans ce modèle, le sunitinib est actif et permet un allongement de la survie des animaux opérés alors que le CVX-241 est sans effet… L’addition de CVX-060 au sunitinib n’améliore pas l’efficacité du sunitinib. Là encore font défaut des éléments thérapeutiques qui auraient été, même redondants, les bienvenus : régorafénib en tant qu’ITK bispécifique, association DC-101–CVX-060 pour distinguer les effets éventuellement multicibles du sunitinib de ses effets anti-angiogéniques, etc. Même en accusant la toxicité des traitements de biaiser les résultats attendus, il est clair que ce modèle ne se comporte pas comme les précédents et ne peut apporter de bases rationnelles à la mise en place d’essais cliniques de l’association, en une ou plusieurs molécules, de l’inhibition de la voie du VEGF et de celle des angiopoïétines.
Commentaires
Bob Kerbel nous a quelque peu habitués à ses effets d’annonce… Il y a dix ans, c’était lui qui proclamait que l’inhibition de l’angiogenèse serait « A cancer therapy resistant to resistance » [6] en raison du fait que les cellules endothéliales, n’ayant pas le phénotype « hypermutateur » des cellules tumorales, seraient incapables d’échapper au traitement anti-angiogénique par des mutations appropriées ; l’avenir lui a donné tort : la redondance (physiologique) des voies de signalisation permet à l’angiogenèse de se produire malgré l’inhibition de l’une d’entre elles… Que le FGF y aille si le VEGF n’y peut aller ! Il nous livre maintenant ses convictions que l’inhibition simultanée de la voie du VEGF et de celle des angiopoïétines permettra d’obtenir une efficacité en situation adjuvante, mais son argumentation expérimentale reste peu convaincante.
La réponse à la question que je posais en guise de titre à cette brève analyse est malheureusement négative : l’utilisation des anti-angiogéniques en situation adjuvante n’est pas pour bientôt. Il sera nécessaire d’approfondir nos connaissances sur l’angiogenèse afin de disposer de bases rationnelles plus solides pour pouvoir lancer de nouveaux essais cliniques. Cependant, la piste ainsi ouverte par le groupe de Kerbel est intéressante et mérite d’être suivie ; nous disposons de très bons modèles in vivo et de molécules innovantes (encore expérimentales pour certaines) ; il faudra sans doute de la ténacité aux équipes cliniques pour progresser dans ce domaine : aujourd’hui, on ne lance des essais thérapeutiques en situation adjuvante que lorsque les traitements ont montré une activité en situation palliative. Il faudra sortir de ce carcan et je ne suis pas certain que les esprits soient préparés à cette révolution copernicienne !
Liens d’intérêts : L’auteur déclare ne pas avoir de lien d’intérêt en rapport avec cet article.